Las leishmaniasis son un grupo de enfermedades originadas por la infección producida por protozoos del género Leishmania, que parasitan las células del sistema reticuloendotelial. Los parásitos son transmitidos por la picadura de las hembras de mosquitos de los géneros Phlebotomus y Lutzomya, de los cuales unas 30 especies son vectores demostrados. El reservorio lo constituyen generalmente mamíferos salvajes o domésticos, aunque también puede ser una infección antroponótica. Su capacidad infectiva se manifiesta de forma variada en la sintomatología, dando lugar a formas viscerales (kala-azar), mucocutáneas y cutáneas.
Epidemiología de la Leishmaniasis
La infección por Leishmania constituye un problema de extraordinaria envergadura desde el punto de vista de la salud pública, ya que afecta a la población de 88 países de zonas intertropicales y templadas, de los cuales sólo en 40 es de declaración obligatoria, por lo que de los aproximadamente 2 millones de casos nuevos estimados por año, sólo 600.000 se declaran oficialmente. La prevalencia está en torno a los 12 millones de enfermos y la población en riesgo es de más de 350 millones de personas.
De los casos nuevos, una cuarta parte corresponden a formas viscerales. En el 90 % en la India, Nepal, Bangladesh, Brasil y Sudán. De las formas cutáneas, el 90 % ocurren en Afganistán, Arabia Saudí, Irán, Siria, Brasil y Perú, y las mucocutáneas se concentran en el 90 % en Bolivia, Brasil y Perú.
La Leishmaniasis en España
En nuestro país, tanto la leishmaniasis cutánea como la visceral están producidas por L. infantum y han sido enfermedades de declaración obligatoria (EDO, rúbrica núm. 085) desde febrero de 1982 hasta el 1 de julio de 1996; a partir de entonces, son enfermedades de notificación regional y sólo se registran en las comunidades autónomas donde se considere oportuno. Por ello no se dispone de una información fiable, aunque la declaración obligatoria previa tampoco reflejaba la realidad por existir una subdeclaración evidente.
De acuerdo con los datos oficiales EDO, las comunidades autónomas más afectadas serían Aragón, Baleares, Cataluña y Valencia y, en un segundo grupo, Andalucía, Castilla-La Mancha y Madrid. Por otra parte, en esta declaración no se diferencia entre leishmaniasis cutánea y kala-azar, por lo que es muy difícil establecer una estimación. Para Alvar, una estimación realista sería de unos 200 casos nuevos viscerales y 100 cutáneos.
De las publicaciones españolas al respecto, señalaremos el trabajo de Albero Blanes et al que recogen 141 casos durante 4 años, en Alcoy; Coscojuela et al 43 casos en 10 años, en Aragón; Alcalde Alonso et al 39 pacientes en 6 años, en Granada, Daudén et al, 31 pacientes en 9 años, en Madrid; y Sesma y Barricarte, 15 casos cutáneos y 18 viscerales en 21 años, en Navarra.
En nuestra consulta, tras una revisión publicada en el año 2000, seguimos intentando recopilar información retrospectiva y actual sobre nuestros pacientes de leishmaniasis. Sobre una población aproximada de 380.000 habitantes, se recogieron, entre 1992 y febrero de 2004, 131 pacientes con lesiones cutáneas o mucosas en los que se confirmó el parásito, de los cuales 125 eran inmunocompetentes, 3 casos de coinfección con virus de la inmunodeficiencia humana (VIH), y otros 3 casos de leishmaniasis de inoculación laríngea, en pacientes inmunocompetentes, atendidos en los servicios de otorrinolaringología (ORL) y medicina interna de nuestro hospital. Si a ello se añaden los casos que sin demostración del parásito presentaban una historia clínica y unas lesiones cutáneas muy sospechosas de botón de Oriente, curados con antimoniales intralesionales, los casos atendidos en otras consultas del área, y un número indeterminado de pacientes que no llegan a las consultas dermatológicas por la regresión espontánea de las lesiones, es muy verosímil que la cifra de pacientes en este periodo pueda incrementarse como mínimo en un 20-25 %. Ello, unido a lo comunicado en las series españolas citadas, hace pensar que la incidencia de la leishmaniasis cutánea en España exceda ampliamente las previsiones de Alvar, que pueden ser mucho más ajustadas en lo que respecta al kala-azar.
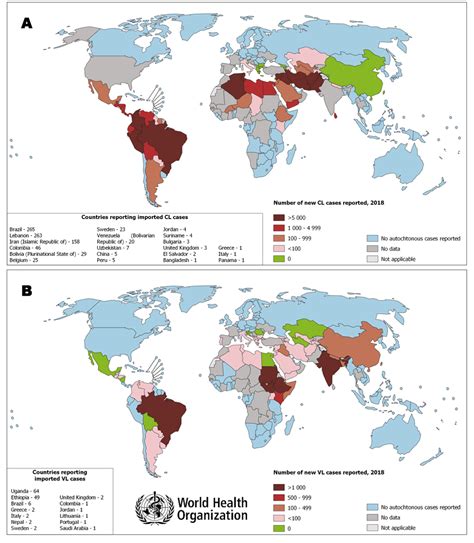
Distribución Mundial de la Leishmaniasis
Historia de la Leishmaniasis
Se conocen referencias de la enfermedad en el papiro de Ebers (hacia 1600 a.C.).
Etiología de la Leishmaniasis
Como se ha dicho en la introducción, el agente causal de las leishmaniasis es un protozoo del género Leishmania pero, como en toda zoonosis, la interacción agente-vector-reservorio es absolutamente determinante para el desencadenamiento de la enfermedad, su transmisión y su mantenimiento como tal en el medio ambiente. Por ello, parece preferible hablar de «complejo etiológico», entendiendo por tal cada uno de esos elementos con sus interrelaciones.
El Parásito
Leishmania, descrita en 1903 por Leishman y Donovan en la India y simultáneamente por Wright en un niño armenio, es un protozoo flagelado perteneciente a la clase Zoomastigophora, orden Kinetoplastida y familia Trypanosomatidae. El género Leishmania (Ross, 1903) incluye más de dos docenas de especies, la mayoría de las cuales parasita al ser humano. De todas ellas, L. donovani (L. archibaldi en el este de África) y L. infantum (L. chagasi en el Nuevo Mundo), tienen un tropismo preferentemente visceral y el resto cutáneo o mucocutáneo. No obstante, algunas de estas especies viscerotrópicas pueden dar lugar a afectación exclusivamente cutánea, como es el caso de L. infantum, agente de la leishmaniasis cutánea en España y en el resto de la cuenca mediterránea occidental y L. chagasi, molecularmente idéntica a L. infantum, también es responsable de formas cutáneas en el Nuevo Mundo. Igualmente se han descrito casos de afectación visceral por L. tropica en zonas endémicas y en veteranos de la guerra del Golfo.
Morfológicamente las leishmanias se presentan bajo una forma intracelular, amastigote, que se encuentra dentro del sistema reticuloendotelial del mamífero huésped, así como en frotis y biopsias y una forma flagelada, promastigote, en el interior del intestino del vector y en los medios de cultivo.
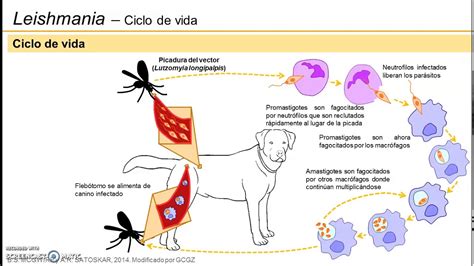
Ciclo de Vida de Leishmania
Los amastigotes se presentan como cuerpos redondeados u ovalados (cuerpos de Leishman-Donovan) de 2-6 mm de diámetro, en los que se identifican un núcleo, un quinetoplasto puntiforme y un flagelo interno, este último sólo visible al microscopio electrónico. La tinción con Giemsa de los frotis obtenidos de las lesiones cutáneas revela un citoplasma azul claro, mientras que el núcleo y quinetoplasto se tiñen de púrpura.
Los promastigotes son alargados, de alrededor de 20 por 2-3 mm, con un núcleo central, un flagelo externo, anterior, rodeado de membrana plasmática, de longitud similar al cuerpo del parásito y un quinetoplasto, ubicado en el extremo anterior, en la proximidad del origen del flagelo.
Desde el punto de vista de su biología molecular y genética, debe señalarse que las leishmanias tienen dos genomas, nuclear y quinetoplástido, este último equivalente al genoma mitocondrial de los mamíferos. El cariotipo de Leishmania es de 34-36 cromosomas, y su tamaño para L. infantum es de 35,5 Mb (Wincker et al, 1996, citado por Alvar) y de 33,6 Mb para L. major (proyecto para estudio del genoma de Leishmania del Centro Sanger).
Ciclo Vital
Leishmania
Para alimentarse, la hembra del insecto vector pica al mamífero reservorio. De este modo, los amastigotes de los tejidos infectados o de la sangre pasan al tracto digestivo del mosquito y en el intestino medio, fundamentalmente, se transforman en promastigotes en 24-36 h tras la picadura, e inician una rápida multiplicación.
Dentro del tubo digestivo del vector, las características del promastigote van cambiando desde la fase de nectomona, sujeto a las microvellosidades del tubo digestivo, a la de promastigote infectivo o metacíclico, libre en hipofaringe, pasando por una fase intermedia de haptomona. Este proceso se conoce como metaciclogénesis y dura aproximadamente 10 días.
Los promastigotes metacíclicos rellenan la faringe y probóscide del mosquito y permanecen allí hasta una nueva picadura, momento en el que serán inoculados a un nuevo huésped. Existe un alto nivel de especificidad entre vector y especie de Leishmania, ligado a la estructura de membrana del parásito y características genéticas del insecto, de modo que una especie de flebótomo sólo es susceptible a una o algunas especies de Leishmania y viceversa.
Con cada picadura entran en la dermis entre 10 y 200 promastigotes metacíclicos, algunos de los cuales, probablemente, son destruidos por los leucocitos polinucleares y eosinófilos, mientras que otros se adhieren a los receptores de superficie de los macrófagos y son fagocitados.
Una vez dentro del macrófago, se transforman nuevamente en amastigotes, que vivirán en los fagolisosomas, o vacuolas parasitóforas del macrófago. En estas estructuras, los amastigotes sobreviven y se multiplican por división binaria, hasta que el macrófago queda repleto de amastigotes, momento en el que se rompe y los parásitos pasan al espacio extracelular, donde serán nuevamente captados por otros macrófagos.
Un factor fundamental asociado a la virulencia es el tropismo de la especie, que hace que las especies viscerotropas L. donovani (L. archibaldi), L. infantum (L. chagasi) alcancen rápidamente cualquier área del sistema reticuloendotelial, mientras que las especies dermotropas como L. tropica o L. major, queden acantonadas preferentemente en piel.
La situación de inmunocompetencia del sujeto infectado también es determinante del alcance de la infección. A este respecto hay que señalar que especies como L. aethiopica o L. major causantes de leishmaniasis cutánea localizada, dan lugar a formas difusas en inmunodeprimidos. Así mismo, las variantes enzimáticas dermotrópicas de L. infantum de la cuenca mediterránea producen leishmaniasis visceral en los inmunodeprimidos, en especial en los infectados por el VIH.
Identificación de las Leishmanias
No existen criterios morfológicos que permitan distinguir las diferentes especies de Leishmania, ni a la observación microscópica convencional de los tejidos parasitados o de los cultivos, ni mediante el estudio de microscopia electrónica, si bien las diferencias que se observan con el microscopio electrónico de transmisión y barrido sugieren diferencias en lo que ocurre a nivel molecular y bioquímico en el momento de la fijación (Blum, 1996).
Por ello, se han propuesto múltiples criterios de identificación, unos extrínsecos, como la sintomatología, distribución geográfica y comportamiento en vectores o animales de laboratorio, y otros intrínsecos que analizan el fenotipo o el genoma del parásito.
Dentro de los criterios extrínsecos, Lainson y Shaw utilizaron el desarrollo de Leishmania en el tubo digestivo del vector para diferenciar las secciones (subgéneros) Suprapylaria (Leishmania) y Peripylaria (Viannia). Las primeras se desarrollarían en el segmento de tubo digestivo anterior al píloro y las segundas en píloro y por detrás del mismo. Así mismo, el vicerotropismo y dermotropismo siguen teniendo vigencia como criterios extrínsecos.
Como criterios intrínsecos, se incluyen las dos técnicas bioquímicas de caracterización fenotípica más utilizadas: la caracterización de isoenzimas y los anticuerpos monoclonales.
La caracterización de isoenzimas se realiza mediante el estudio de la movilidad electroforética de estas enzimas en cultivos de promastigotes de diferentes estirpes de Leishmania. Ello permite la caracterización de éstas, según sus perfiles enzimáticos, en grupos taxonómicos electroforéticamente homogéneos llamados zimodemos. Es la técnica de referencia en la actualidad para la identificación de leishmanias a niveles específicos e intraespecíficos.
El uso de anticuerpos monoclonales contra antígenos específicos de género o de especie de Leishmania permite identificar amastigotes en frotis y biopsias, o promastigotes en cultivos.
Sin embargo, el desarrollo de la biología molecular ha permitido la puesta en marcha de numerosas técnicas de identificación molecular, que permiten la identificación del genoma, de mayor sensibilidad y especificidad que las técnicas extrínsecas. Con este propósito se utiliza el aislamiento de fragmentos específicos de ADN mediante enzimas de restricción (RFLP), hibridación con sondas de ADN genómico y el ADNk del quinetoplasto y la reacción en cadena de la polimerasa (PCR) con sus variantes RAPD (random amplified polimorphic DNA) y PCR-RFLP, que identifica y diferencia estirpes genéticamente próximas. La Leishmania Genoma Network (Red para del estudio del genoma de la Leishmania) agrupa a varios centros actualmente ocupados en secuenciar el genoma del protozoo.
Clasificación
La clasificación del género Leishmania, establecida por Ross en 1903, comenzó en 1916 y ha seguido los pasos basados en los diferentes criterios de identificación antes mencionados. Hasta 1961, las diferentes clasificaciones siguen el sistema de Linneo basándose en características biogeográficas y clínicas y, posteriormente, se van añadiendo aspectos de comportamiento del parásito en vectores, cultivos y animales de experimentación.
Las técnicas de identificación de características bioquímicas, en particular las isoenzimas, dieron paso a clasificaciones filogenéticas en las que los caracteres biológicos se ordenan de acuerdo con la evolución, para conseguir diseñar un árbol filogenético (cladograma, dendrograma), en el que se muestra la sucesión de ancestros y descendientes.
El uso actual de técnicas moleculares, en particular la secuenciación genómica de Leishmania, permite completar y precisar las clasificaciones actualmente vigentes.
Desde el punto de vista práctico, se adoptará la clasificación que muestra la tabla en la que se correlaciona la especie con el tropismo y patología habitual que produce, referida a las especies más frecuentes de Leishmania.
El Vector
Los vectores de las leishmaniasis son mosquitos del orden Dipterae, familia Psychodidae, subfamilia Phlebotominae y géneros Phlebotomus (12 subgéneros), en el Viejo Mundo y Lutzomya (25 subgéneros), en el Nuevo Mundo. La identificación de los flebotominos como vectores fue llevada a cabo, por primera vez, por Adler y Theodor en 1925.
Excepcionalmente se ha comunicado la transmisión ac...

Phlebotomus papatasi
tags: #dermatologue #montpellier #pages #jaunes