La necesidad de alcanzar tanto la óptima localización en la arcada del implante como el eje, dirección y nivel de emergencia adecuados, ha estimulado la búsqueda y desarrollo de numerosos materiales capaces de sustituir al hueso para tratar defectos óseos de diferente etiología, magnitud y localización.
En el presente trabajo se realiza una revisión bibliográfica de los sustitutos no óseos disponibles en el mercado para mejorar y acelerar la regeneración ósea centrándonos en los polímeros de ácido poliláctico y poliglicólico por su relativa novedad para dicha aplicación.
Para que se produzca el crecimiento óseo en un defecto es necesario que exista un coágulo sanguíneo, la conservación de los osteoblastos y el contacto con el tejido vivo.
Los mecanismos biológicos que participan en la neoformación ósea varían según el tipo de injerto que se emplee y podríamos resumirlos en:
- Osteogénesis: formación de hueso nuevo por las células que sobreviven en el injerto. Esta actividad se produce principalmente en las cuatro primeras semanas tras la colocación del mismo. El injerto de hueso esponjoso trabecular es más osteogénico que el cortical ya que presenta mayor cantidad de células osteoprogenitoras. Sin embargo, hay que destacar que sólo sobrevivirán las células que se encuentren a menos de 300 µm de una fuente de aporte sanguíneo, mientras que todas las demás células morirán antes de que les lleguen los nutrientes necesarios por difusión.
- Osteoconducción: el injerto sirve de guía para el crecimiento óseo ya que es progresivamente colonizado por vasos sanguíneos y células osteoprogenitoras de la zona receptora, que van lentamente reabsorbiéndolo y depositando hueso nuevo. Esta propiedad la poseen el hueso autólogo, la hidroxiapatita reabsorbible, el hueso desmineralizado y los cristales bioactivos entre otros.
- Osteoinducción: transformación de las células mesenquimales indiferenciadas perivasculares de la zona receptora en células osteoformadoras. Esta fase comienza a las dos semanas de la colocación del injerto y alcanza su máximo nivel entre las seis semanas y los seis meses posteriores, disminuyendo más tarde de forma progresiva. Esta propiedad la poseen las proteínas morfogenéticas óseas (BMPs) y diversos factores de crecimiento como TGF-ß.
Los tres mecanismos ocurren simultáneamente siempre y cuando se trate de un injerto de hueso autólogo.
El autoinjerto es considerado por la mayoría de los autores el injerto ideal por su comportamiento en la mayoría de las situaciones. Es osteogénico, pues contiene células vitales y proteínas morfogenéticas y no existe posibilidad de que provoque reacciones inmunitarias adversas.
Presenta una serie de desventajas como la morbilidad intrínseca en su obtención, morfología, gran coste económico y disponibilidad limitada sobre todo en cirugía pediátrica.
Estos inconvenientes unidos a la posible reabsorción ósea al cabo del tiempo, han desencadenado el desarrollo vertiginoso de los sustitutos no óseos en los que se engloban: los materiales biocerámicos, los cristales bioactivos y los polímeros.
Materiales Biocerámicos
El hueso es una estructura compuesta de células, agua, matriz orgánica y sales inorgánicas. El componente inorgánico del hueso representa aproximadamente el 70% de su peso seco, es biocompatible, no es inmunógeno y está constituido por sales de calcio, fundamentalmente fosfato de calcio, junto con pequeñas cantidades de sodio y magnesio. Las sales de calcio, y en particular la hidroxiapatita y el carbonato de calcio son bioactivas y osteoconductoras.
Fosfato Tricálcico
Con la fórmula Ca3(PO4)2, tiene una relación calcio-fosfato de 1,51 a diferencia de la hidroxiapatita cuya proporción calcio-fosfato es de 1,67 lo que les otorga una diferente aceptación e integración biológica.
Es biodegradable por una combinación de disolución fisicoquímica y fragmentación. Es una cerámica porosa, osteoconductora y se reabsorbe rápidamente por lo que el hueso formado es débil para asegurar un papel mecánico importante.
Gauthier y cols. han demostrado en distintos estudios experimentales realizados en perros beagle su eficacia en el mantenimiento de la cresta alveolar tras la extracción dentaria o en la regeneración ósea de defectos periimplantarios.
Es un material de relleno parcialmente reabsorbible que ha mostrado resultados clínicos aleatorios y es fácil encontrarlo encapsulado por tejido conjuntivo fibroso. Alguno de los nombres comerciales serían el cemento Norian CRS® (Synthes Maxillofacial, West Chester, PA).
Hidroxiapatita
Con la fórmula Ca10 (PO4)6 (OH)2 puede ser de origen natural: bovina (Bio-Oss®), equina (Bio-Gen®), coralina (HAP-200®) y ficógena (Algipore®) o de origen sintético (cerámica o no cerámica). La hidroxiapatita sintética es porosa, tiene una estructura compuesta por calcio, fósforo e iones hidroxilo, compatible con los tejidos vivos y estructura similar al hueso; es estéril, osteoconductiva y posee una excelente osteointegración.
Como nombres comerciales destacar:
- OsteoGraf/N® (CeraMed, Lakewood, CO). Es una hidroxiapatita reabsorbible obtenida mediante métodos físicos. Es biocompatible, macro y microporosa. Existen dos granulometrías: 420-1.000 mm (Osteo Graf/N-700®) y 250-420 mm (OsteoGraf/N-300®). Hay un OsteoGraf asociado con un péptido sintético (P-15) análogo del colágeno (OsteoGraf/N P-15®). Es una hidroxiapatita no cerámica, reabsorbible, altamente hidrofílica.
- Calcitite® (Zimmer Dental). Es una hidroxiapatita cerámica, no reabsorbible compuesta por partículas de forma esférica.
La seguridad y efectividad de la hidroxiapatita han sido confirmadas en experimentos animales con ratas Wistar y conejos de Nueva Zelanda y en un amplio rango de campos clínicos, incluyendo la cirugía plástica, la cirugía ortopédica, la neurocirugía y la cirugía bucal.
Como ventajas derivadas de la utilización de este material destacamos: no necesitar una segunda cirugía para su retirada, lo que reduce la morbilidad y riesgo del paciente; fácil manipulación y obtención y, debido a su contenido en calcio resulta un material radiodenso que nos permite realizar controles radiográficos.
Entre las desventajas de la hidroxiapatita se encuentran su débil resistencia mecánica y fragilidad.
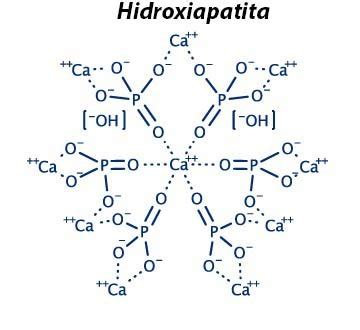
Estructura de Hidroxiapatita
Cristales Bioactivos
Hench fue el pionero del desarrollo de las cerámicas de vidrio describiéndolas como sustancias bioactivas. Un estudio realizado por Schmitt muestra como los cristales bioactivos en cultivo con osteoblastos in vitro expresan gran cantidad de fosfatasas alcalinas, lo que es indicativo de alta actividad osteoblástica, mayor que la que expresa la hidroxiapatita en las mismas condiciones pero in vivo se comportan peor.
Actualmente se encuentran disponibles en el mercado dos formas de cristales bioactivos: PerioGlas® (US Biomaterials Corp. Alachua, FL) y Biogran® (Orthovita, Malvern, PA), formados por partículas de Bioglass® (45% SiO2, 24,5% Na2O, 24,5% CaO y 6% P2O5) de diferente tamaño. PerioGlas® tiene un rango de tamaño de partícula de 90 a 710 µm y Biogran® lo tiene de 300 a 355 µm.
Schepers y Ducheyne observaron en un estudio realizado en mandíbulas de perros que a los tres meses de la implantación de partículas de Bioglass® en defectos óseos se producía neoformación ósea no solo a partir de las paredes del defecto sino por el interior del mismo lo que viene a significar que este material tiene propiedades osteogénicas.
Furusawa y cols. en un estudio realizado en la zona posterior mandibular de 18 ratas Wistar demostraron la capacidad osteoconductiva del Biogran®, capaz de formar hueso a las cuatro semanas de la intervención.
Este mismo autor con alguno de sus colaboradores, en un estudio publicado un año antes, habla de las ventajas y desventajas de distintos tipos de biomateriales sintéticos así como de la formación ósea dual inducida por dicho biomaterial.
Para estos investigadores, el Biogran® se diferencia del resto de materiales sintéticos porque en contacto con el tejido óseo se muestra osteoconductor, iniciándose este crecimiento óseo desde la periferia de los gránulos pero, el crecimiento óseo también se observa desde el centro de los gránulos localizados a distancia del hueso preexistente.
Estudios realizados por Fetner y cols. sobre defectos periodontales en monos mostraron que las partículas de Bioglass® tenían mayor capacidad osteoconductora que el fosfato tricálcico y la hidroxiapatita sintética a los cuatro meses de la implantación de los biomateriales. Los porcentajes de nuevo hueso en los diferentes grupos de estudio fueron: 47% Bioglass®, 31% el fosfato tricálcico, 18% la hidroxiapatita sintética y 21% el grupo control.
En este trabajo los autores destacan además la capacidad del Bioglass® para inhibir el crecimiento epitelial en las bolsas periodontales.

Micrografía de Bioglass
Polímeros
Los polímeros ofrecen una alternativa sintética para la regeneración ósea, clasificándose en reabsorbibles y no reabsorbibles.
Polímeros No Reabsorbibles: HTR
El polímero no reabsorbible y poroso (reposicionador de tejido duro) es un material desarrollado por Ashman en 1985. Combina polimetilmetacrilato (PMMA) con polihidroxil-etilmetacrilato (PHEMA). Es un polímero fuerte, microporoso, hidrofílico, fácil de usar, biocompatible y radiopaco. Es osteoconductor y osteogénico.
Según el autor es capaz de promover la regeneración de hueso al humedecerse con médula ósea sangrante, porque el HTR actúa sobre las células pluripotenciales de la médula para que se diferencien en osteoblastos y se forme hueso.
Comercialmente se presenta en dos formas: HTR 24 recomendado para mantenimiento de la cresta y su aumento y HTR 40 recomendado para usar alrededor del implante y en defectos periodontales.
En el estudio publicado por Martínez-González y cols. se evalúa el comportamiento histológico presentado por este material en la reparación de defectos óseos creados en las extremidades posteriores de doce conejos encontrando resultados similares en el proceso reparativo entre el grupo control donde no existía ningún material implantado y el grupo correspondiente al polímero HTR.
Según los autores, este biomaterial no disminuye el tiempo de cicatrización ósea en condiciones fisiológicas pero sí confirman su biocompatibilidad así como sus propiedades osteoconductoras favoreciendo el desarrollo trabecular de hueso neoformado en forma de red intergranular.
Polímeros Reabsorbibles
Dentro de los polímeros reabsorbibles, destacan el ácido poliglicólico (PGA), el ácido poliláctico (PLA) y el ácido poliláctico-poliglicólico (PLGA).
Ácido láctico Para La Piel ¿Qué es y cómo se usa?
1. Ácido Poliglicólico (PGA)
Es el poliéster alifático lineal más simple. Fue utilizado para desarrollar la primera sutura sintética totalmente absorbible y se comercializó como Dexon® en los años 60 por Davis & Geck, Inc (Danbury, CT). Mediante un proceso de dimerización del ácido glicólico se sintetiza el ácido monómero el cual, por polimerización de apertura del anillo, produce un material de alto peso molecular y con un porcentaje de 1-3% de monómero residual.
Su característica principal es su elevada cristalinidad (45-55%) que le permite alcanzar una temperatura de fusión de 230º C.
No es soluble en muchos solventes orgánicos, a excepción de organofluorados como el hexafluoroisopropanol. Las fibras obtenidas a partir de PGA tienen un elevado módulo de Young y resistencia. Su rigidez dificulta su uso para suturas, excepto cuando se emplea como material trenzado.
Las suturas de PGA pierden alrededor del 50% de su resistencia después de dos semanas y el 100% en un mes. Son completamente absorbidas en 4-6 meses.
El poliglicólico ha sido copolimerizado con otros monómeros para reducir la rigidez de sus fibras.
2. Ácido Poliláctico (PLA)
Se obtiene mediante polimerización por apertura de anillo del dímero cíclico del ácido láctico. El monómero tiene un carbono asimétrico por lo que es factible preparar polímeros con diferentes tacticidades. El homopolímero derivado del monómero natural L-láctico (L-PLA) presenta un elevado grado de cristalinidad (37%) debido a su estereorregularidad.
El material tiene alta tensión y baja elongación lo que se traduce en un elevado módulo de Young. El polímero es muy adecuado para aplicaciones que tienen que soportar una carga como son las suturas y fijaciones ortopédicas. Sus características térmicas están definidas por un elevado punto de fusión (175-178º C) y una temperatura de transición vítrea de 60-65º C.
El D-L-poliláctico es un polímero amorfo ya que está constituido por las dos formas isoméricas (D-L) del ácido láctico. En este caso el polímero tiene baja resistencia a la tensión, alta elongación y una elevada velocidad de degradación que hace que sea un material muy atractivo para los sistemas de liberación de fármacos.
Se preparan también copolímeros de L-PLA y D,L-PLA para disminuir la cristalinidad del polímero quiral y acelerar el proceso de degradación. Se ha empleado en forma de membrana (Atrisorb®, Epi-Guide®) para la regeneración ósea guiada con resultados clínicos equivalentes entre ellas y las de PTFE.
3. Ácido Poliláctico-Poliglicólico (PLGA)
Los polímeros de ácido poliláctico y poliglicólico se han constituido en diferentes proporciones que muestran distintos tiempos de reabsorción que pueden oscilar entre dos y treinta y seis meses como se muestra en la siguiente tabla:
| Composición | Tiempo de Reabsorción (meses) |
|---|---|
| D, L-láctico y poliglicólico (50:50) | 2-3 |
| Poliglicólico | 3-4 |
| D, L-láctico y poliglicólico (85:15) | 2-4 |
| Poli (D, L-láctico) | 4-6 |
| Poli (L-láctico) | 18-36 |
Debido a sus propiedades biológicas y mecánicas los polímeros de ácido poliláctico o los copolímeros PLA y PG tienen desde hace varios años aplicaciones terapéuticas muy diversas.
El PLGA se sintetiza mediante copolimerización de apertura en anillo de dos monómeros diferentes, los dímeros cíclicos (1,4-dioxano-2,5-diones) del ácido glicólico y el ácido láctico. Los polímeros pueden sintetizarse como copolímeros aleatorios o en bloque, lo que les confiere propiedades poliméricas adicionales.
Entre los catalizadores habituales utilizados en la preparación de este polímero se encuentran el 2-etilhexanoato de estaño(II), los alcóxidos de estaño(II) o el isopropóxido de aluminio.
En función de la proporción de lactida y glicolida utilizada para la polimerización, pueden obtenerse diferentes formas de PLGA: éstas suelen identificarse con respecto a la proporción molar de los monómeros utilizados (por ejemplo, PLGA 75:25 identifica un copolímero cuya composición es 75% de ácido láctico y 25% de ácido glicólico).
La cristalinidad de los PLGA variará de totalmente amorfa a totalmente cristalina, dependiendo de la estructura del bloque y de la proporción molar. Los PLGA suelen tener una temperatura de transición vítrea de entre 40 y 60 °C.
Los PLGA pueden disolverse con una amplia gama de disolventes, dependiendo de su composición. Los polímeros de lactida superiores pueden disolverse utilizando disolventes clorados, mientras que los materiales de glicolida superiores requerirán el uso de disolventes fluorados como el HFIP.
El PLGA se degrada por hidrólisis de sus enlaces éster en presencia de agua. Se ha demostrado que el tiempo necesario para la degradación del PLGA está relacionado con la proporción de monómeros utilizados en la producción: cuanto mayor es el contenido de unidades de glicólido, menor es el tiempo necesario para la degradación en comparación con los materiales predominantemente láctidos. Una excepción a esta regla es el copolímero con una proporción de monómeros de 50:50, que presenta una degradación más rápida (unos dos meses).
El PLGA se hidroliza en el organismo para producir los monómeros originales: ácido láctico y ácido glicólico. Estos dos monómeros, en condiciones fisiológicas normales, son subproductos de diversas vías metabólicas del organismo. El ácido láctico se metaboliza en el ciclo del ácido tricarboxílico y se elimina a través de dióxido de carbono y agua.
El cuerpo también puede metabolizar los dos monómeros, lo que en el caso del ácido glicólico produce pequeñas cantidades de ácido oxálico tóxico, aunque las cantidades producidas por las aplicaciones típicas son minúsculas y la toxicidad sistémica asociada al uso de PLGA para aplicaciones biomateriales es mínima. En general, el PLGA se considera bastante biocompatible.
La biocompatibilidad del PLGA se ha comprobado tanto in vivo como in vitro. La biocompatibilidad de este polímero viene determinada generalmente por los productos en los que se degrada, así como por la velocidad de degradación en productos de degradación. La forma en que el PLGA se degrada es por medio de una enzima conocida como esterasa, que forma ácido láctico y ácido glicólico.
Aunque los subproductos no suelen acumularse en el organismo, hay casos en los que estos subproductos (ácido láctico y glicólico) pueden ser peligrosos para el organismo cuando se acumulan en altas concentraciones locales. También puede haber pequeños trozos de los polímeros a medida que el polímero se degrada, lo que provoca una respuesta inmunitaria por parte de los macrófagos.
Estos efectos adversos pueden reducirse utilizando concentraciones más bajas del polímero, de modo que se libere de forma natural por todo el organismo. La biodegradación del PLGA lo hace útil para multitud de prácticas médicas.
Se ha desarrollado otra forma inyectable de PLGA con sistemas de erosión. Esta forma puede utilizarse en el medicamento Lupron Depot. Para conseguirlo, el PLGA se mezcla con un disolvente orgánico miscible en agua aprobado por la Food and Drug Administration (FDA). Una vez que el PLGA se mezcla en el disolvente con el fármaco elegido para crear una solución o suspensión homogénea. Cuando se inyecta esta mezcla, el PLGA se solidifica debido a su insolubilidad en agua y es sustituido por el agua. Lentamente, el fármaco se libera de la solución.
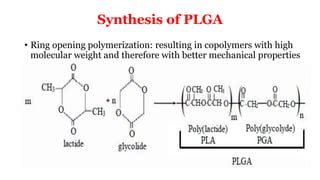
Estructura de PLGA
Los resultados obtenidos permiten confirmar la capacidad osteoconductora de dichos sustitutos en los procesos reparativos óseos pero a menudo también pueden actuar como barrera del proceso fisiológico de autorremodelación ósea al requerir un tiempo de reabsorción demasiado largo.