Los pacientes con psoriasis saben que esta enfermedad dermatológica, además de los problemas generales en su piel, también les aumenta el riesgo de desarrollar otras patologías como enfermedades cardiovasculares, renales, alteraciones psiquiátricas y síndrome metabólico. Ese mayor riesgo está demostrado por la evidencia científica.
En los últimos años, se ha descubierto que esta condición dermatológica, crónica y hereditaria, también está íntimamente relacionada con enfermedades inflamatorias intestinales, como la colitis ulcerosa y la enfermedad de Crohn.
En este sentido, según un nuevo estudio, la inflamación de la piel puede tener un impacto en el intestino, de ahí que pacientes con psoriasis corran más riesgo de sufrir enfermedad de Crohn, además de síntomas gastrointestinales, como dolor y distensión abdominal.
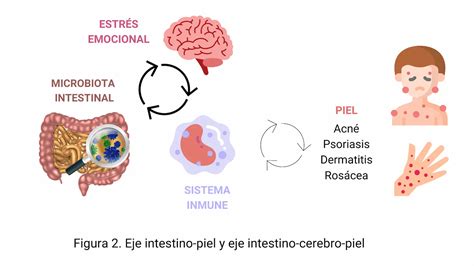
Conexión entre el intestino y la piel en pacientes con psoriasis.
La Inflamación Intestinal y la Psoriasis
La psoriasis es una enfermedad cutánea inflamatoria crónica que cada vez se reconoce más como una enfermedad sistémica. Además de los síntomas cutáneos típicos, los afectados a menudo presentan síntomas acompañantes en otros sistemas de órganos, especialmente en el intestino. Esta conexión plantea nuevas preguntas sobre la fisiopatología y posibles enfoques terapéuticos.
Estudios sugieren que los pacientes con psoriasis tienen un mayor riesgo de enfermedades intestinales inflamatorias como enfermedad de Crohn o colitis ulcerosa. Sin embargo, incluso sin enfermedades intestinales manifiestas, muchos afectados experimentan síntomas como flatulencia, dolor abdominal o diarrea.
Nuevos Hallazgos Sobre Inflamaciones Intestinales Subclínicas
Un estudio reciente examinó el intestino de pacientes con psoriasis sin enfermedades intestinales visibles y se encontraron cambios significativos en la mucosa intestinal. En particular, el número de células inmunitarias activadas como los granulocitos eosinófilos, los macrófagos y las células T CD8+ fue mayor en comparación con los controles sanos.
Además, aproximadamente la mitad de los pacientes con psoriasis tenían una permeabilidad intestinal aumentada. Esta alteración de la permeabilidad se correlacionó con niveles elevados de citocinas (incluyendo IL-17A e IL-13) y síntomas gastrointestinales.
- Granulocitos eosinófilos: La densidad de estas células inmunitarias fue significativamente mayor en el duodeno de pacientes con psoriasis. Además, mostraron marcadores de actividad aumentada como CD66b, que indican activación celular y degranulación.
- Mastocitos: Se encontró un mayor número de mastocitos en el duodeno, pero sin evidencia de una actividad aumentada.
- Macrófagos: Los investigadores observaron un cambio hacia macrófagos proinflamatorios M1, que son conocidos por su papel en las inflamaciones crónicas.
- Células T CD8+: Estas células no solo estaban aumentadas, sino que también mostraron marcadores de actividad elevada como CD69 y CXCR3. Esto sugiere un papel central en el proceso inflamatorio.
La barrera intestinal juega un papel central en la protección contra microorganismos patógenos y toxinas. Una permeabilidad aumentada, como se observó en los pacientes estudiados, podría promover la entrada de mediadores inflamatorios en el sistema circulatorio sistémico.
La consecuencia: reacciones inflamatorias subclínicas, pero sistémicas, que no solo afectan el intestino, sino también otros órganos. Es especialmente notable la correlación entre la función de barrera alterada y los síntomas como flatulencia o dolor abdominal, incluso sin una enfermedad intestinal visible.
El Intestino Permeable y la Inflamación
En algunas enfermedades autoinmunes, la mucosa intestinal, que protege frente a infecciones y permite que los nutrientes y el agua pasen a través de ella, no funciona correctamente. Cuando no hace su función de barrera, las bacterias y las sustancias nocivas tienen más facilidad para filtrarse, lo que provoca inflamación del intestino y, a su vez, puede causar una inflamación más generalizada cuando estas sustancias llegan al torrente sanguíneo. Es lo que de denomina "intestino permeable".
Los investigadores observaron que la mitad de los pacientes con psoriasis del ensayo presentaban intestino permeable y que, a su vez, eran los que tenían más síntomas gastrointestinales, como dolor abdominal y distensión abdominal. Además, presentaban niveles elevados de sustancias inflamatorias en sus intestinos.
"Dado que los pacientes con psoriasis de nuestro estudio tenían una enfermedad cutánea relativamente leve y no mostraban inflamación intestinal visible en una gastroscopia, presentaban cambios sorprendentemente claros en su intestino delgado en comparación con los controles sanos. Estos cambios podrían explicar por qué los pacientes con psoriasis a menudo tienen problemas gastrointestinales y un mayor riesgo de desarrollar la enfermedad de Crohn", ha detallado la especialista.
Estudio Analiza la Relación Entre Psoriasis y Enfermedad Inflamatoria Intestinal
En este sentido, un grupo de dermatólogos analizó más de 1.100 registros y evaluó cinco estudios controlados y cuatro estudios de cohorte, lo que supuso tener en cuenta datos de casi ocho millones de personas. Tras analizar los resultados, se ha podido comprobar que los pacientes con psoriasis que participaron en los estudios controlados (más rigurosos que los de cohortes u observacionales) tuvieron un riesgo 1,7 veces mayor de desarrollar enfermedad de Crohn y de 1,75 de sufrir colitis ulcerosa en comparación a personas sin psoriasis.
En relación con la base genética, los autores del estudio apuntan a alteraciones en los genes IL12B e IL23R, este último afecta a la producción de interleuquina 17, cuya unión con su receptor estimula la hiperproliferación y diferenciación de queratinocitos, la maduración de las células dendríticas y el reclutamiento de neutrófilos y macrófagos en lesiones psoriásicas.
Por otro lado, señalan estos autores, la piel y el intestino tiene similitudes en psoriasis y enfermedad inflamatoria intestinal, incluyendo una inmensa diversidad microbiana y un abundante suministro en sangre.
Por último, los autores del estudio señalan algunas limitaciones de este trabajo como que sólo se incluyera en la revisión un estudio cohorte en el que se informara de una asociación entre diferente gravedad de psoriasis y enfermedad inflamatoria intestinal.
Por otro lado, sólo había un estudio controlado con pacientes asiáticos, que fue precisamente el que no mostró un mayor riesgo de enfermedad inflamatoria intestinal en personas con psoriasis. Por este motivo, los dermatólogos del Chang Gung Memorial Hospital consideran que se requieren más estudios en esta población para confirmar este hecho.
MICROBIOTA ⚠️ PROBLEMAS de la PIEL y DISBIOSIS intestinal
La Importancia de la Microbiota Intestinal
Seguramente no se conoce popularmente, pero todos los microbios que habitan en el intestino representan alrededor de un kilo de lo que se pesa en total. Esta población de bacterias es lo que se conoce como microbiota intestinal y en los últimos años ha demostrado ser tan importante, que algunos investigadores hablan de ella como un “nuevo órgano” o “segundo cerebro” del ser humano.
Sí: ese ecosistema autosostenible de “bichos” que quizá le resultan repugnantes es necesario para el buen funcionamiento del organismo. “Hasta ahora conocemos poco porque hace solo 10 años que se estudia la microbiota humana aplicada a la medicina.
“En neurología también hay descrita una relación entre la microbiota y la enfermedad. Sobre todo, en la esclerosis múltiple, aunque se está empezando a investigar esta relación en el párkinson, el alzhéimer, la epilepsia y el autismo. Y también en otras patologías inflamatorias, como la enfermedad de Crohn [una inflamación crónica del tracto intestinal] o la celiaquía. Son un grupo muy diverso de enfermedades que en general comparten un mecanismo inmunológico-alérgico.
Todas estas enfermedades, además, tienen una similitud: son propias de los países desarrollados (especialmente las de tipo inmunológico-alérgico) y, también, mucho más prevalentes en las últimas décadas.
“Por eso se piensa que hay un componente en la dieta de las personas -la comida tiene “bichos”, gérmenes- que hace que estas enfermedades aparezcan. Quienes vivimos en países desarrollados tenemos el mismo número de bacterias en el intestino que los países menos desarrollados, pero mucha menos biodiversidad. Nuestra biodiversidad es casi la mitad que la de ellos.
Suscribe esta idea Francisco Guarner, investigador del VHIR (Vall d’Hebron Institut de Recerca) del grupo de fisiología y fisiopatología digestiva, quien asegura que actualmente “hay enfermedades por falta de bacterias”.
“Hemos dejado de dar de comer a nuestras bacterias ‘buenas’. Cuando solo comemos pan blanco, huevo o carne y renunciamos a los vegetales, lo absorbemos todo nosotros y no damos trabajo a esas bacterias buenas, que acaban atrofiándose.

La microbiota intestinal y su impacto en la salud.
¿Es Posible Revertir Estas Dolencias Modificando la Microbiota?
Pero, si la microbiota intestinal alterada se relaciona con la aparición de enfermedades, ¿es posible revertir estas dolencias modificando la microbiota?
“En la soriasis solo hay un ensayo clínico que demuestra que con un preparado probiótico concreto [los probióticos son microorganismos vivos que pueden estar en los alimentos, medicamentos o complementos de la dieta], a las 12 semanas, el paciente tiende a normalizar la microbiota y, con ello, la enfermedad mejora”, comenta el doctor Navarro. También con la celiaquía en niños se han hecho avances.
“La enfermedad mejora con probióticos. Hay un estudio realizado hace tres años en EEUU sobre autismo -los pacientes con autismo tienen la microbiota alterada- y parece ser que con el uso de una mezcla probiótica disminuye la agresividad e hiperactividad de estos niños”, añade Navarro. Sin embargo, no es posible de momento revertir el trastorno del espectro autista.
En esclerosis múltiple no hay ensayos clínicos que incluyan un gran número de pacientes para intentar modificar esa microbiota. Sí hay estudios de laboratorio con ratas en los que se demuestra que, cuando se les hace una transposición de heces de pacientes con esclerosis múltiple, estas ratas empiezan a desarrollar la enfermedad. Todos estos hallazgos, no obstante, señalan un camino por el que seguir.
“Son nuevas vías terapéuticas. Estamos hablando de enfermedades de causa multifactorial. Esto es, sabemos que hay componentes hereditarios, inflamatorios, de medio ambiente, autoinmunes… Y parece que uno de esos componentes es la microbiota intestinal.
El mismo explica que el 57% de los genes que tenemos en el cuerpo son bacterianos: es decir, las bacterias han logrado incrustar parte de su material genético en nuestro código genético y actualmente representan más que nuestros genes humanos.
“Está claro que tanta bacteria tiene que estar implicada en la salud y enfermedad. Se ha demostrado que el intestino influye en la piel y en el cerebro”, dice el doctor.
¿Por qué? “Porque en el intestino tenemos el 80% del sistema linfático, los ganglios sin activar están en la mucosa intestinal. El intestino es, después del cerebro, el órgano que más neuronas tiene: por eso también se conoce como el “segundo cerebro” del ser humano.
“El intestino tiene toda una red de neuronas conectadas capaces de tomar decisiones sin contar con el cerebro. El 99% de lo que hace el intestino lo decide hacer él solo”, señala Francisco Guarner, investigador del VHIR (Vall d’Hebron Institut de Recerca) del grupo de fisiología y fisiopatología digestiva.
Un ejemplo: cuando una persona vive una situación de estrés, es frecuente que el intestino grueso provoque una diarrea. “El intestino sabe que estás estresado y prefiere vaciar, así como también cierra un poco el estómago. ¿Entonces pueden nuestras emociones afectar al sistema digestivo? Algunas sí.
“El estrés es una emoción muy estudiada porque se da en otros mamíferos. También influye el placer: hay muchas vías de placer que comienzan en el intestino y van hacia el cerebro”, cuenta Guarner.
La Hipótesis de la Higiene y las Plagas Modernas
Según explica Martin J. Blaiser en el libro ‘SOS Microbios’ (Debate), las “plagas modernas” (obesidad, diabetes infantil, asma, fiebre del heno, alergias a determinados alimentos, reflujo esofágico, cáncer, enfermedad celíaca, enfermedad de Crohn, colitis ulcerosa, autismo, eczemas) tienen que ver, para muchas personas, con la “hipótesis de la higiene”. Es decir, muchos padres creen que, debido a que “hemos dejado el mundo demasiado limpio”, los sistemas inmunitarios de los hijos se han quedado inactivos.
Para este médico las causas de estas enfermedades son “el uso excesivo de antibióticos en humanos y animales, las cesáreas y el uso generalizado de desinfectantes y antisépticos”. También advierte de que la pérdida de diversidad de nuestro microbioma “afecta al metabolismo, la inmunidad y la cognición”.
“Si no cambiamos nuestros hábitos, nos veremos en una situación aún peor. Los microbios, dice Blaiser, ayudan a mantener estable la presión arterial a través de receptores especializados ubicados en los vasos sanguíneos. “Estos sensores detectan pequeñas moléculas creadas por los microbios que recubren el intestino. Su respuesta a estas moléculas regula la presión arterial. Así, después de comer, la tensión puede bajar”, dice Blaiser.
Enfoque en la Salud Intestinal Necesario
El estudio destaca que la psoriasis debe entenderse como una enfermedad sistémica en la que la salud intestinal juega un papel importante. Los hallazgos sugieren que la estabilización de la barrera intestinal o la modulación inmunológica específica en el intestino podrían desempeñar un papel en la terapia en el futuro.
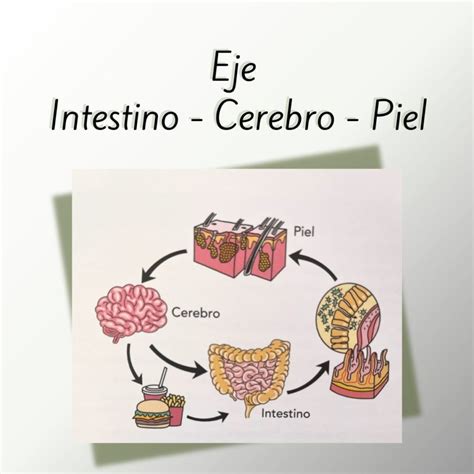
El eje intestino-piel y su relación con la salud.
tags: #psoriasis #y #problemas #digestivos