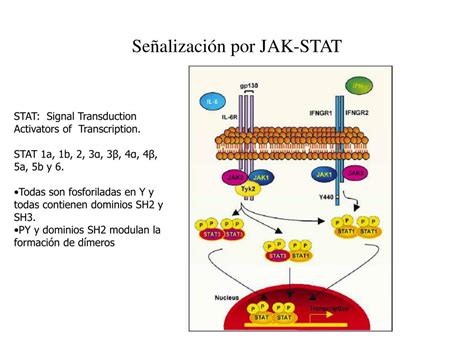
La vía de señalización de citocinas Janus cinasa/transductor de señal y activador de transcripción (JAK/STAT) es un área de interés emergente en dermatología, con evidencia creciente del papel clave en la patogénesis de las enfermedades inflamatorias cutáneas. Debido a que algunas citocinas proinflamatorias usan la vía JAK/STAT para la transducción de señales, se convierte en una diana terapéutica prometedora para el tratamiento de dichas enfermedades al modular de forma selectiva el sistema inmune.
El objetivo de esta revisión es conocer la vía de señalización JAK/STAT y su papel en distintas enfermedades dermatológicas inmunomediadas. En esta segunda parte, se revisará la eficacia y seguridad de los inhibidores de JAK -en formulación oral o tópica- para el tratamiento de la psoriasis, la dermatitis atópica y otras dermatosis.
En la parte 1 de esta revisión se ha descrito de forma detallada la familia de las Janus cinasas (JAK) y la vía de señalización intracelular Janus kinase/signal transducer and activator of transcription (JAK/STAT). Se ha destacado el papel que podrían tener los inhibidores de JAK (JAKi) en el tratamiento de distintas enfermedades inflamatorias dermatológicas, revisando específicamente la evidencia actual disponible en vitíligo y alopecia areata.
En esta parte 2 se realiza una revisión de la patogénesis y el papel de la vía JAK/STAT en psoriasis y dermatitis atópica y también otras dermatosis como la hidrosadenitis, la dermatomiositis o la enfermedad de injerto contra húesped, entre otras.
Artritis psoriásica: Cómo diferenciarla de la artritis reumatoide y la osteoartritis
Psoriasis y la Vía JAK/STAT
Aunque el eje interleucina-23/interleucina-17 (IL-23/IL-17) se considera actualmente la vía patogénica principal en la psoriasis, en esta enfermedad intervienen numerosas citocinas, algunas de las cuales transmiten su señal tras la unión a los correspondientes receptores a través de la vía JAK/STAT: el interferón gamma (IFN-γ), el interferón alfa (IFN- α), la IL-2, la IL-6, la IL-12, la IL-13, la IL-19, la IL-20, la IL-21, la IL-22 y la IL-23.
El factor de necrosis tumoral alfa (TNF-α) y otras citocinas, como la IL-17, la IL-8 o las de la familia IL-1 (IL-1, IL-18, IL-36 e IL-38) no activan directamente la vía JAK/STAT pero su actividad se puede suprimir indirectamente mediante la inhibición de la vía JAK/STAT.
Se ha demostrado una sobrerregulación de la señalización JAK con un incremento en la expresión de STAT1 y STAT3 en las lesiones de psoriasis cuando se comparan con piel sana.
STAT1 es responsable de la transducción de señales del IFN tipo I (α y β) y tipo II (γ) a través de un mecanismo dependiente de JAK1/JAK2, llevando a la producción de múltiples mediadores proinflamatorios y la activación y maduración de las células dendríticas con estimulación de linfocitos Th1 y Th17.
A través de la activación de JAK2/TYK2 inducida por IL-23, STAT3 está involucrada en la inducción y diferenciación de las células Th17. Adicionalmente las células Th17 pueden producir IL-22, responsable de hiperplasia epidérmica y producción de péptidos antimicrobianos por los queratinocitos.
STAT3 participa también en la proliferación de queratinocitos a través de la activación de JAK1/JAK2 o JAK1/TYK2 inducida por IL-6. Además, IL-17 activa de forma indirecta STAT3 a través de la inducción de IL-19 y/o IL-36 por los queratinocitos.
Las investigaciones actuales se centran en los inhibidores de TYK2 para el tratamiento de la psoriasis moderada a grave.
La proporción de pacientes que alcanzó PASI75 a las 12 semanas en un ensayo en fase II con 267 pacientes fue significativamente superior con deucravacitinib (un inhibidor de TYK2, Bristol-Myers Squibb) que con placebo (39% a dosis de 3mg/24h, 69% a dosis de 3mg/12h, 67% a dosis de 6mg/12h y 75% a dosis de 12mg/24h, en comparación con 7% en el grupo placebo). La tasa de respuesta PASI90 fue 43% a las 12 semanas, y la tasa de respuesta PASI100 fue del 25%.
Actualmente, hay tres ensayos de fase III en curso con este fármaco (NCT04036435, NCT03924427), uno de ellos comparándolo con apremilast (NCT03611751).
Brepocitinib (Pfizer), un inhibidor potente de TYK2/JAK1, se está evaluando como tratamiento de la psoriasis. En un ensayo en fase I, 30 pacientes con psoriasis en placas moderada a grave recibieron 30mg o 100mg oralmente o placebo una vez al día durante 28 días. La respuesta PGA0/1 se consiguió en el 57,1%, 100% y 0% de los casos respectivamente.
Su aplicación tópica se está testando actualmente en un ensayo en fase IIb en pacientes con psoriasis leve a moderada (NCT03850483).
Finalmente, se está investigando otro inhibidor de TYK2 (PF-06826647, Pfizer) para psoriasis moderada a grave en un ensayo en fase II (NCT03895372).
Inhibidores de JAK: Tofacitinib
Tofacitinib (Xeljanz®, Pfizer) inhibe primariamente JAK1 y JAK3. Está aprobado por la FDA para el tratamiento de pacientes adultos con artritis psoriásica (PsA) y para el tratamiento de la artritis reumatoide moderada a grave a dosis de 5mg dos veces al día. Recientemente ha sido aprobada para el tratamiento de la artritis idiopática juvenil poliarticular en niños de 2 años o más, y también para el tratamiento de la colitis ulcerosa a dosis de 10mg dos veces al día durante 8 semanas y posteriormente 5mg dos veces al día.
Tofacitinib ha demostrado eficacia en psoriasis moderada-grave en ensayos en fase II y III.
En 197 pacientes tratados con tofacitinib 2mg, 5mg y 15mg dos veces al día se consiguió a las 12 semanas una respuesta Psoriasis Area and Severity Index 75 (PASI75) del 25%, 41% y 67% respectivamente, en comparación con el 2% del placebo. El 22% de los pacientes que recibieron tofacitinib consiguieron una respuesta PASI90 en la semana 12.
En un ensayo de fase III que incluyó a 1106 pacientes con psoriasis en placas con PASI de 12 o superior se demostró la no inferioridad de tofacitinib 10mg/12h frente a etanercept 50mg subcutáneo en la semana 12, con una tasa de efectos adversos similar en ambos grupos.
En dos ensayos de fase III (OPT pivotal 1 -incluyendo 901 pacientes- y OPT pivotal 2 -con 960 pacientes-), tofacitinib 10mg/12h fue más eficaz que 5mg/12h a partir de la semana 16, con una mayor tasa de respuesta PASI75 entre las semanas 16 a 28. Entre los pacientes que consiguieron PASI75 en la semana 16, el 74,1% del grupo de 5mg/12h y el 79,4% del grupo 10mg/12h mantuvieron la respuesta a las 52 semanas y la mayoría lo seguían haciendo a los 24 meses.
Además, a las 16 semanas de tratamiento ambas dosis produjeron mejoría en la psoriasis ungueal, el prurito (la diferencia se hacía evidente un día después del inicio del tratamiento) y el Dermatology Life Quality Index, con mantenimiento de la mejoría a la semana 52.
En otro ensayo en fase III en la semana 16 se consiguió una respuesta American College of Rheumatology 20 (ACR20) en todos los pacientes con PsA tratados con tofacitinib (5mg/12h o 10mg/12h), y una respuesta ACR50 o ACR70 en más de la mitad. Las respuestas se mantuvieron en la semana 52.
La mayoría de los efectos adversos presentados fueron leves o moderados. En los grupos de tofacitinib doce pacientes tuvieron herpes zóster, aunque el efecto adverso más frecuente fue la nasofaringitis.
Dos pacientes tratados con tofacitinib 10mg cada 12h presentaron infecciones graves (apendicitis, neumonía y pielonefritis) en OPT Pivotal 1, mientras que tres pacientes que recibieron tofacitinib 5mg cada 12h presentaron infecciones graves (neumonía, herpes zóster, erisipela) en OPT Pivotal 2. En ambos estudios describen incremento en las cifras de colesterol, creatina fosfocinasa (CPK) y disminución de la hemoglobina.
Los efectos adversos de tofacitinib son similares con dosis de 5mg y 10mg, siendo los más frecuentes citopenias leves, infecciones del tracto respiratorio superior (IRVA), cefalea, infección del tracto urinario y diarrea.
En octubre de 2015, la FDA rechazó la autorización de tofacitinib para el tratamiento de la psoriasis en placas moderada a grave alegando que eran precisos más estudios sobre su seguridad a largo plazo.
Tofacitinib Tópico
Tofacitinib tópico podría ser una alternativa terapéutica para psoriasis en placas leve a moderada, con un perfil de seguridad favorable, aunque la mejoría ha sido discreta en los estudios publicados. En un estudio en fase IIa con 71 pacientes se encontraron resultados prometedores con pomada de tofacitinib al 2%/12h.
El cambio porcentual respecto al valor inicial en la semana 4 en la puntuación de gravedad de placa objetivo (TPSS) fue estadísticamente significativo con la pomada de tofacitinib en comparación con el vehículo (promedio de mínimos cuadrados -54,4% vs.-41,5%, respectivamente).
Posteriormente, se llevó a cabo un estudio aleatorizado multicéntrico incluyendo 435 pacientes, en el que tofacitinib en pomada al 1% y al 2% demostraron más eficacia que el vehículo para el tratamiento de la psoriasis en la semana 8 (Physician's Global Assessment-PGA-0/1 en el 18,6% para tofacitinib 2% cada 24h y en el 22,5% para tofacitinib 2% cada 12h), pero no en la semana 12. El 8,1% de los pacientes tuvieron reacciones en el sitio de aplicación, aunque la mayor incidencia fue en el grupo vehículo.
Ruxolitinib Tópico
Ruxolitinib, un inhibidor de JAK1/2, se ha estudiado en el tratamiento tópico de la psoriasis. En un ensayo clínico en fase II, 29 pacientes se aleatorizaron a recibir ruxolitinib crema al 0,5% o al 1% una vez al día o al 1,5% dos veces al día 28 días, vehículo o un comparador activo (crema de calcipotrieno 0,005% o betametasona dipropionato 0,05%).
El tratamiento con ruxolitinib crema al 1% y 1,5% fue seguro, bien tolerado y efectivo, con reducción en el grosor de las placas, el eritema, la descamación y el área de la lesión en comparación con el vehículo (reducción del 53% en los grupos de tratamiento vs. 32% del vehículo). No se encontraron diferencias significativas en cuanto a eficacia entre ruxolitinib y los comparadores activos.
Baricitinib Oral
Baricitinib, un inhibidor de JAK1/2 (Olumiant®, Lilly), está aprobado por la FDA y la European Medicines Agency (EMA) para el tratamiento de la artritis reumatoide moderada a grave con dosis recomendadas de 4mg al día. Recientemente ha recibido la aprobación para el tratamiento de la dermatitis atópica moderada a grave.
Se ha estudiado en un ensayo en fase IIb para el tratamiento de la psoriasis en placas moderada a grave en 271 pacientes. La respuesta PASI75 en la semana 12 fue significativamente superior para el grupo tratado con 8mg y de 10mg una vez al día en comparación con placebo (42,9%, 54,1% y 16,1%, respectivamente).
Los efectos adversos más frecuentemente observados fueron las infecciones, con una tasa de incidencia del 26,5% en el grupo placebo y del 21,5% para los grupos de baricitinib, siendo la más común la nasofaringitis.
Abrocitinib Oral
Abrocitinib (Pfizer) es un inhibidor de JAK1 que se ha evaluado para el tratamiento de la psoriasis moderada a grave en un ensayo en fase II de 12 semanas de duración, asignando 59 pacientes en total a recibir aleatoriamente 200mg/24h, 400mg/24h o 200mg/12h o placebo durante 4 semanas.
En la semana 4, la proporción de pacientes que consiguieron una respuesta PASI75 fue de 17% para placebo y 200mg/24h, 50% para 400mg/24h y 60% para 200mg/12h. Se observaron más anormalidades analíticas (neutropenia, trombocitopenia, reticulopenia) en el grupo 200mg/12h, pero sin infecciones graves ni hemorragias asociadas.
Solcitinib Oral
Se ha descrito una mejoría de la psoriasis dependiente de la dosis con Solcitinib (GlaxoSmithKline), un inhibidor JAK1 que se ha ensayado en fase II. Se incluyeron 60 pacientes y se observaron respuestas PASI75 del 13% con dosis de 100mg/día, 25% con dosis de 200mg/día, 57% con dosis de 400mg/día y 0% con placebo.
Itacitinib Adipato Oral
Itacitinib adipato (Incyte Corporation), un inhibidor JAK1, demostró mejoría significativa en pacientes con psoriasis moderada a grave en un ensayo en fase II de 12 semanas de duración que incluyó a 50 pacientes. La tasa de respuesta PASI75 al cabo de un mes fue de 0%, 11,1%, 0%, 22,2% y 27,7% en los grupos placebo, itacitinib 100mg/24h, 200mg/24h, 200mg/12h y 600mg/24h, respectivamente.
Los pacientes recibieron tratamiento activo (10mg, 25mg, 60mg, 100mg dos veces al día o 50mg una vez al día) o placebo. El promedio de mejoría en PASI y Body Surface Area (BSA) con respecto al valor basal fue significativamente superior en todos los grupos de tratamiento en comparación con el grupo placebo a las 6 semanas, de forma dependiente de la dosis.
Dermatitis Atópica y la Vía JAK/STAT
La dermatitis atópica (DA) es una enfermedad inflamatoria cutánea con una respuesta inmune polarizada con predominio Th2 en su fase aguda. La vía JAK/STAT juega un papel esencial en la disregulación de la respuesta inmune en la DA, incluyendo la sobrerregulación de la respuesta Th2, la activación de los eosinófilos, la supresión de las células T reguladoras (Treg) y la maduración de las células B, con diferenciación a células plasmáticas y secreción de inmunoglobulina E (IgE) que se une a los mastocitos cutáneos y causa liberación de histamina.
La respuesta Th2 produce asimismo liberación de citocinas proinflamatorias y factores proangiogénicos por las células epidérmicas.
La DA se asocia a un incremento en la señalización a través de JAK1, JAK2, JAK3 y TYK2. JAK1, JAK3 y STAT6 son componentes de la señalización IL-4 críticos para la diferenciación Th2 y la producción de IL-4, IL-5, IL-10, e IL-13.
STAT6 regula los genes involucrados en Th2 y diferenciación de células B, el switching de IgG a IgE y la producción de moléculas del complejo mayor de histocompatibilidad de clase II. Diversos polimorfismos de STAT6 se han relacionado con una mayor susceptibilidad a la DA y presencia de niveles elevados de IgE.
La vía IL-4/IL-13/JAK/STAT es importante para la integridad de la barrera cutánea. Se ha demostrado que la supresión mediante un JAKi no selectivo de la activación de STAT3 inducida por IL-4/IL-13 mejora la función de barrera, promoviendo la producción de filagrina y loricrina.
Además, IL-4 e IL-13 también intervienen en el prurito mediante sus interacciones con IL-4Rα y JAK1 en las neuronas sensoriales.
Inhibidores de JAK orales y tópicos para enfermedades de la piel
En el ámbito de las enfermedades inflamatorias crónicas de la piel (IMIDs), los inhibidores de JAK orales y tópicos se están utilizando cada vez más. La Administración de Alimentos y Medicamentos (FDA) ha aprobado su uso en dermatitis atópica (Upadacitinib, Abrocitinib y Ruxolitinib), vitíligo (Ruxolitinib) y alopecia areata (Baricitinib, Ritlecitinib). A pesar de que los inhibidores de JAK muestran una alta eficacia, su perfil de seguridad sigue siendo un punto de discusión, especialmente en lo que respecta al posible aumento del riesgo de eventos cardiovasculares graves y tromboembólicos venosos.
Una revisión ahora ha examinado si el uso de inhibidores de JAK en indicaciones dermatológicas conlleva un mayor riesgo de eventos cardiovasculares y tromboembólicos. Para ello, se evaluaron datos de 35 estudios controlados aleatorizados y de 20.651 pacientes. Los pacientes padecían dermatitis atópica, psoriasis (incluida la artritis psoriásica), alopecia areata o vitíligo. La proporción de mujeres y hombres fue aproximadamente igual (mujeres: 46%, hombres: 56%), y la edad media fue de 38,5 años.
Resultados de la revisión
El análisis no mostró diferencias significativas en cuanto a eventos cardiovasculares graves y mortalidad total entre los inhibidores de JAK y el placebo o las sustancias de comparación. Las análisis de subgrupos adicionales (inhibidores de JAK orales vs. tópicos vs. diferentes enfermedades) produjeron resultados similares.
Tampoco se encontraron diferencias significativas entre los inhibidores de JAK y el placebo o las otras sustancias de comparación en cuanto a los eventos tromboembólicos venosos.
Los autores concluyeron que los inhibidores de JAK pueden ser una valiosa opción adicional para los pacientes con enfermedades inflamatorias autoinmunes que no responden a las estrategias de tratamiento tradicionales. Sin embargo, también señalaron los resultados del estudio ORAL Surveillance, que mostró un mayor riesgo de eventos cardiovasculares y tromboembólicos graves, así como de aparición de tumores.
En este estudio, sin embargo, solo participaron pacientes mayores (edad media 61 años) con artritis reumatoide, tratamiento con metotrexato concomitante y al menos un factor de riesgo cardiovascular. Además, los períodos de observación de ambos estudios difirieron significativamente. Mientras que la revisión tenía una duración media de seguimiento de 4,9 meses, el estudio ORAL Surveillance se extendió durante cuatro años.
Para evaluar de manera más completa la seguridad y los riesgos a largo plazo de los inhibidores de JAK en enfermedades inflamatorias autoinmunes, se necesitan más estudios con períodos de observación más largos.
Consideraciones Adicionales sobre Tofacitinib
El tofacitinib no ha sido estudiado, y por ello se debe evitar su utilización en combinación con medicamentos biológicos, tales como los antagonistas del TNF, los antagonistas de la interleucina (IL)-1R, los antagonistas de la IL-6R, los anticuerpos monoclonales anti-CD20, los antagonistas de la IL-17, los antagonistas de la IL-12/IL-23, los antagonistas de las integrinas, los moduladores selectivos de la coestimulación y los inmunosupresores potentes, tales como azatioprina, 6-mercaptopurina, ciclosporina y tacrolimus, debido a la posibilidad de un aumento de la inmunosupresión y un mayor riesgo de infección.
Ha habido una mayor incidencia de reacciones adversas con la combinación de tofacitinib y metrotexato (MTX) frente a tofacitinib en monoterapia en los ensayos clínicos de AR.
Riesgos Asociados a Tofacitinib
- Tromboembolismo venoso (TEV): Se han observado acontecimientos graves de TEV incluido embolismo pulmonar (EP), algunos de los cuales fueron mortales, y trombosis venosa profunda (TVP) en pacientes en tratamiento con tofacitinib. Tofacitinib se debe usar con precaución en pacientes con factores de riesgo conocidos de TEV, independientemente de la indicación y la dosis.
- Infecciones graves: Se han notificado infecciones graves y en ocasiones mortales debido a bacterias, micobacterias, hongos invasivos, virus u otros patógenos oportunistas en pacientes que toman tofacitinib. No se debe comenzar el tratamiento con tofacitinib en pacientes con infecciones activas, incluidas las infecciones localizadas.
- Tuberculosis: Se deben considerar los riesgos y beneficios antes de comenzar el tratamiento con tofacitinib en pacientes que hayan estado expuestos a la tuberculosis, que hayan residido o viajado a regiones endémicas de tuberculosis.
- Reactivación viral: Se ha observado reactivación viral y casos de reactivación del virus del herpes (por ejemplo, herpes zóster) en los ensayos clínicos con tofacitinib.
- Neoplasia maligna y trastorno linfoproliferativo: Se deben considerar los riesgos y beneficios del tratamiento con tofacitinib antes de comenzar la terapia en pacientes con presencia o antecedentes de neoplasias malignas distintas a un cáncer de piel no melanoma (CPNM) tratado con éxito.
- Cáncer de piel no melanoma (CPNM): Se ha notificado CPNM en pacientes tratados con tofacitinib. El riesgo de CPNM puede ser mayor en pacientes tratados con tofacitinib 10 mg dos veces al día que en pacientes tratados con 5 mg dos veces al día.
- Enfermedad pulmonar intersticial: Se han notificado acontecimientos de enfermedad pulmonar intersticial (algunos con resultado de muerte) en pacientes tratados con tofacitinib en ensayos clínicos de AR y en la fase posterior a la comercialización.
- Perforaciones gastrointestinales: Se han notificado casos de perforación gastrointestinal en ensayos clínicos, aunque se desconoce el papel de la inhibición de la JAK en estos casos.
- Riesgo cardiovascular: Los pacientes con AR y APs tienen un mayor riesgo de padecer trastornos cardiovasculares.
- Enzimas hepáticas: El tratamiento con tofacitinib se ha relacionado con un aumento de las enzimas hepáticas en algunos pacientes.
- Hipersensibilidad: Se han notificado casos de hipersensibilidad asociada a la administración de tofacitinib.
Parámetros Analíticos y Precauciones
- Linfocitos: No se recomienda comenzar o continuar el tratamiento con tofacitinib en pacientes con un recuento de linfocitos confirmado inferior a 750 células/mm3.
- Neutrófilos: No se recomienda comenzar el tratamiento con tofacitinib en pacientes con un RAN inferior a 1.000 células/mm3.
- Hemoglobina: No se recomienda comenzar el tratamiento con tofacitinib en pacientes con un valor de hemoglobina inferior a 9 g/dl.
- Control de lípidos: El tratamiento con tofacitinib se relacionó con un aumento en los parámetros lipídicos tales como colesterol total, colesterol asociado a lipoproteínas de baja densidad (LDL) y colesterol asociado a lipoproteínas de alta densidad (HDL).
- Vacunas: No se recomienda administrar vacunas de microorganismos vivos simultáneamente con tofacitinib.
| Inhibidor de JAK | Aprobación FDA | Indicaciones | Dosis Común |
|---|---|---|---|
| Tofacitinib | Sí | Artritis Psoriásica, Artritis Reumatoide, Colitis Ulcerosa | 5mg dos veces al día |
| Baricitinib | Sí | Artritis Reumatoide, Dermatitis Atópica | 4mg al día |
| Ruxolitinib (tópico) | Sí | Dermatitis Atópica | Aplicación tópica según indicación |
tags: #anti #jak #rhumatisme #psoriasique