Los avances en la fisiopatología de las enfermedades inflamatorias y autoinmunes han potenciado el conocimiento del papel de las células T y de las citocinas derivadas de células T en la generación de inflamación tisular. Aunque el posible origen inmunológico de la psoriasis sigue todavía en discusión, lo que sí es indudable es que los fenómenos inmunológicos desempeñan un papel relevante.
La infiltración por linfocitos, la secreción de diversas citocinas y quimiocinas, etc., son elementos importantes en la fisiopatología de la enfermedad. Esto ha llevado a diseñar estrategias de interferencia en estos procesos que pueden llevar a dar una solución a la psoriasis.
Desde un punto de vista teórico, el mecanismo de interferencia más directo sería la utilización de anticuerpos monoclonales (acm) que actúen directamente sobre dianas de las células efectoras o sobre los mecanismos de reconocimiento celular. En este aspecto no sólo el linfocito, sino tanto las células presentadoras de antígeno como los queratinocitos, pueden desempeñar un papel en la inmunopatogénesis de la psoriasis, ampliando el número de objetivos a los que pueden ser dirigidos los tratamientos. Además se pueden utilizar como dianas las citocinas que las células utilizan en su actividad inflamatoria o efectora.
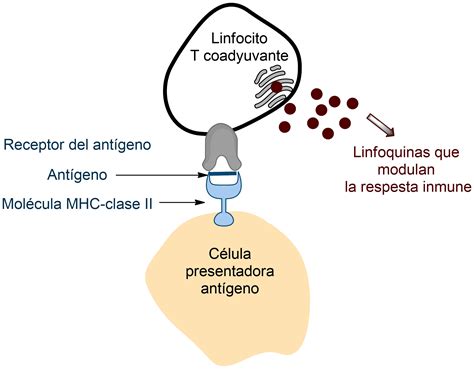
Interacción entre el linfocito T y la célula presentadora de antígeno.
El primer acm usado terapéuticamente en humanos fue el OKT3 (anti-CD3). Sin embargo, aunque eficaz, su uso estaba asociado a graves e incluso mortales efectos secundarios debidos a síntomas de la enfermedad del suero y del síndrome de liberación de citocinas. Además, debido a que provocaba una profunda inmunosupresión, se produjo un aumento de infecciones y a largo plazo el desarrollo de enfermedades linfoproliferativas.
Asimismo, tanto este acm como la mayor parte de los primeros acm ensayados eran usados directamente tras ser generados en ratones, por lo que los pacientes desarrollaban anticuerpos contra inmunoglobulinas de ratón que a veces influían en el efecto del anticuerpo.
Esto llevó a la realización de cambios en las tecnologías de preparación de acm (anticuerpos quiméricos, humanizados y humanos) y a la búsqueda de moléculas no inmunoglobulinas que tuvieran una alta afinidad por receptores celulares y pudieran interferir en su actividad.
Nuevas Tecnologías en la Preparación de Anticuerpos Monoclonales
Brevemente explicaremos estas nuevas tecnologías:
- Anticuerpos Quiméricos: Son anticuerpos en los que la parte variable de la inmunoglobulina de ratón se une a una región constante de inmunoglobulina humana. Esto reduce la inmunogenicidad de los anticuerpos.
- Anticuerpos Humanizados: Se consiguen mediante ingeniería genética. En este caso sólo las regiones determinantes del reconocimiento antigénico de las regiones variables del anticuerpo de ratón se combinan con la estructura de la región variable humana. Estos anticuerpos deben ser más «humanos» que los anticuerpos quiméricos y quizá menos inmunogénicos.
- Anticuerpos Humanos: Se pueden conseguir mediante tres técnicas: donantes inmunizados, de librerías de fagos y de ratones transgénicos que sólo sintetizan inmunoglobulinas humanas.
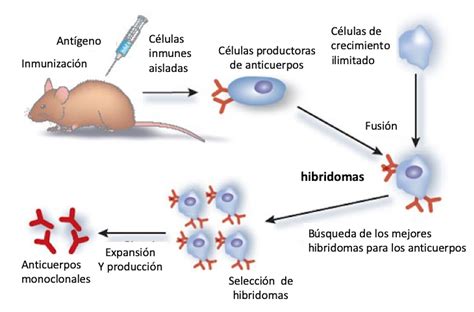
Anticuerpos monoclonales del ratón al humano.
Otras alternativas para interferir en los mecanismos de reconocimiento o activación celular son:
- Los ligandos: se usan ligandos de receptores celulares para bloquear el receptor o receptores solubles de citocinas para captar la citocina e impedir que llegue a su receptor natural. En muchas ocasiones el ligando se une a un cuerpo de inmunoglobulina que facilita que la sustancia permanezca más tiempo en el torrente sanguíneo sin ser eliminada por los mecanismos de detoxificación y que no sea reconocida como inmunógeno.
- Los inmunoconjugados: se obtienen de fusionar, bien por una reacción química, bien mediante ingeniería genética, un acm o un ligando con una toxina (botulínica, colérica) capaz de destruir la célula diana.
Revisaremos las diversas estrategias utilizadas y los resultados obtenidos con relación al tratamiento de la psoriasis. Muchos de los anticuerpos están en desarrollo y sometidos a estudios clínicos, por lo que los resultados todavía no son públicos y sólo se dispone de la información que publicita la compañía farmacéutica. Siempre que ha sido posible hemos reflejado la dosificación, vía de administración, resultados con relación al PASI, los efectos secundarios clínicos y analíticos.
Tratamiento del cáncer con anticuerpos monoclonales
Anticuerpos Monoclonales Específicos y sus Aplicaciones
Anti-CD2
CD2 es un antígeno de superficie de los linfocitos T que media la adhesión a las células presentadoras de antígeno, donde su ligando es CD58 (LFA-3).
Amevive® (alefacept, LFA3TIP) es la fusión de LFA-3, ligando de CD2, con una IgG1 humana, por lo que no es un acm. Con esta molécula se han desarrollado diversos ensayos clínicos y se han tratado un número alto de pacientes (al menos 600 al completar los estudios de fase II). En uno de los estudios en fase II, multicéntrico, doble ciego, se incluyeron 229 pacientes tratados con tres dosis distintas de LFA3TIP intravenosos semanales durante 12 semanas frente a placebo.
El tratamiento fue bien tolerado, sin observarse efectos secundarios importantes y con mejoría significativa de la psoriasis. Se produjo una disminución en linfocitos CD4 a expensas de los CD4+ CD45RO+ (células T de memoria y efectoras) y sólo un paciente desarrolló anticuerpos contra el LFA3TIP sin relevancia clínica.
Se ha finalizado un estudio de fase III, multicéntrico, multinacional, doble ciego, comparando dosis de 10 y 15 mg de alefacept con placebo, administrado intramuscularmente una vez por semana durante 12 semanas, con un seguimiento posterior de 12 semanas más. Se incluyeron 507 pacientes y se obtuvo mejoría significativa en los pacientes tratados, sobre todo con la dosis de 15 mg. Se alcanzó una reducción del 75% del PASI en un 33% y de más del 50% en un 57%, con mínimos efectos secundarios (no hubo signos o síntomas de inmunosupresión) y una reducción significativa de CD4.
Llamativamente, los pacientes que lograron una reducción del PASI mayor del 75% mantenían una reducción del mismo superior al 50% después de 7 meses tras el tratamiento. No se observó ni efecto rebote ni reactivación de la psoriasis.
Siplizumab (MEDI-507) es un anticuerpo humanizado anti-CD2 derivado del anticuerpo murino BTI-322. Se han realizado ensayos clínicos abiertos de fase 1 con dosis única intravenosa en 14 pacientes, de fase I/II con dosis intravenosa semanal durante 8 semanas en 26 pacientes y de fase I/II con diversas dosis subcutáneas semanales durante 12 semanas en 39 pacientes. Globalmente más del 70% de pacientes tuvieron una reducción del PASI superior al 25%. En el grupo de dosis más alta un 39% de pacientes presentó una reducción del 75% y un 55% más del 50%. Se han iniciado dos ensayos clínicos de fase II en abril de 2001 con pacientes de Europa (que se había completado en septiembre con 121 pacientes) y EE.UU. (donde se espera incluir 400 pacientes). En estos ensayos se utilizan inyecciones subcutáneas semanales durante 12 semanas.
Anti-CD3
CD3 es un antígeno presente en todos los linfocitos T que forma un complejo con el receptor de células T (TCR). La activación de las células T depende de la interacción del complejo TCR/CD3 con su ligando.
Como hemos indicado previamente el acm anti-CD3 IgG2a Orthoclone® OKT3 obtenido en ratones fue utilizado en pacientes con trasplante renal, hepático o cardíaco con graves efectos secundarios e incluso mortales: fiebre, distrés respiratorio, síndrome de liberación de citocinas y aumento en la incidencia de infecciones y de enfermedades linfoproliferativas, estos últimos probablemente debidos a su gran efecto inmunosupresor.
Debido a estos problemas se han desarrollado otros acm que reconocen otros epítopos en CD3 y se han ensayado sobre todo en pacientes sometidos a trasplantes. Se ha publicado un único paciente tratado con OKT3 debido a una esclerosis múltiple y que además padecía psoriasis. Durante el tratamiento se observó una mejoría rápida (10 días) de su enfermedad.
Nuvion® es un acm IgG2 humanizado HuM291 anti-CD3 (SMART anti-CD3) en el que se han realizado modificaciones para evitar el síndrome de liberación de citocinas, con el que recientemente se han iniciado estudios en fase I/II.
Anti-CD4
CD4 es una molécula importante en la regulación de la inmunidad. Participa en el reconocimiento de los antígenos de histocompatibilidad de clase II. En la mayor parte de los infiltrados inflamatorios dérmicos se encuentra una preponderancia de linfocitos CD4, por lo que bloquear la activación de estas células parece un camino para disminuir la reacción inflamatoria.
La publicación en 1991 de una observación aislada del efecto de un acm anti-CD4 en un paciente con psoriasis desencadenó la publicación de otros casos tratados con anti-CD4.
El tratamiento con acm anti-CD4 se había empleado previamente en trasplante y en enfermedades autoinmunes como la artritis reumatoide, así como en tratamientos contra el virus de la inmunodeficiencia humana. Se han utilizado diversos acm con distintas especificidades. Presenta pocos efectos secundarios y se han observado anticuerpos neutralizantes en una baja proporción de pacientes.
Las series publicadas han demostrado cierta eficacia en el tratamiento de la psoriasis. Así, la primera serie publicada fue con el acm BB14/BF15, una IgG1 murina de líquido ascítico que fue utilizado en tres pacientes durante 8 días. Los pacientes sufrieron fiebre, escalofríos y en un caso cefalea y dolor abdominal, sugestivos de una enfermedad del suero. El PASI mejoró en los tres con un máximo a los 20-30 días y rebrote al cabo de 1 mes. No se evidenciaron alteraciones humorales significativas, ni siquiera una disminución del número de linfocitos CD4+, aunque todos generaron anticuerpos contra el acm.
El acm quimérico M-T413 (IgG1 humana) se ha utilizado en un paciente con psoriasis pustuloso durante 1 semana con buena respuesta. Se objetivó una linfopenia con disminución en el número de linfocitos CD4.
Con el acm murino YNB46.1.8, humanizado con IgG1, se realizó tratamiento intravenoso en diversas dosis y pautas en cinco pacientes. Un paciente mejoró mucho (75% de reducción del PASI) y cuatro parcialmente (reducción del 20%-40%). De los tres pacientes con artropatía psoriásica, dos notaron una mejoría articular que duró de 1 a 3 meses. En la primera dosis todos los pacientes sufrieron de fiebre, escalofríos y en algunos casos hipotensión y dolor torácico que no ocurrió con las siguientes dosis y que se interpretaron como una liberación de citocinas en respuesta al acm. Se produjo una disminución del número de CD4 (30%-70%) que se recuperó lentamente y no se observó la producción de anticuerpos contra el acm. Globalmente se produjo una mejoría transitoria que fue algo más prolongada en la afectación articular.
Otro abordaje, usando un acm murino OKT4A humanizado con IgG4 se aplicó sobre seis pacientes. Se obtuvo una reducción del 46% a las 4 semanas, que permaneció similar durante 6 meses en cuatro pacientes. Un paciente no respondió al tratamiento y el otro sufrió un rebrote de sus lesiones. No se objetivaron efectos secundarios, excepto prurito en dos pacientes, ni cambios analíticos, permaneciendo estables el número de CD4 y sin aparición de anticuerpos contra el acm.
Humax-T4® es un acm humano contra CD4 del que está en desarrollo un estudio en fase II desde enero de 2001. Recientemente han informado de una reducción del 30% del PASI, estadísticamente significativa, en los pacientes tratados. El fármaco fue seguro y bien tolerado.
Anti-CD6
La glucoproteína CD6 es una molécula accesoria que media la activación y proliferación de células T. Algunos anti-CD6 han sido usados en tratamiento de enfermedad injerto contra huésped y en linfoma de células T. Hay un caso publicado de tratamiento intravenoso con un acm IgG2 murino anti-CD6 junto con una formulación tópica del mismo acm. La paciente mejoró de sus lesiones.
Anti-CD11a
LFA-1 es un heterodímero de CD11a y CD18 que se expresa en todos los linfocitos.
LFA-1 es el ligando de ICAM-1 y funciona como molécula coestimuladora para la activación de los linfocitos.
Xanelim® (efalizumab, hu1124) es un acm humanizado del acm murino anti-CD11a MHM24. Se han tratado 31 pacientes en un estudio abierto con diversas dosis intravenosas únicas. Se observó un aumento de eficacia con mayor dosis, así hubo dos respuestas parciales entre los ocho pacientes tratados con dosis menores a 0,3 mg/kg, tres parciales y cinco completas en los quince tratados con dosis medias y una parcial y cuatro completas en los cinco tratados con más de 1,0 mg/kg. En pacientes tratados con dosis menores a 0,6 mg/kg los efectos secundarios fueron mínimos, pero en el grupo con dosis mayores sufrieron cefaleas y escalofríos (56%), rebrote de psoriasis, fiebre (40%), infecciones y náuseas (27%) en las 24 h tras la infusión. No se objetivó una disminución en los linfocitos T o B.
En estudio en fase I/II abierto con 61 pacientes con dosis inicial subcutánea de 0,7 mg/kg, seguido de once inyecciones subcutáneas semanales en dosis de 1 a 4 mg/kg se observó una mejoría del 50% o más del PASI en un 75% de los pacientes y una mejoría del 75% o más en un 31%. Se comprobó que la dosificación subcutánea tenía características farmacocinéticas y farmacodinámicas similares a la formulación intravenosa, manteniéndose niveles adecuados del fármaco durante el tratamiento. El tratamiento fue bien tolerado, observándose cefaleas, síntomas gripales y síntomas de psoriasis. No se observó ningún efecto grave.
Tratamientos Sistémicos Innovadores para la Psoriasis
Los innovadores tratamientos sistémicos para la psoriasis son un excelente ejemplo de medicina traslacional. En las últimas décadas se ha avanzado considerablemente en la elucidación de la compleja y multifactorial patogenia de la psoriasis como base para el desarrollo de opciones terapéuticas altamente eficaces . Hoy en día, a nivel celular y molecular, se considera que el patomecanismo esencial es una respuesta inmunitaria mediada por células T y un medio de citocinas característico asociado.
A nivel genético, se han identificado numerosos loci genéticos asociados a la psoriasis. El HLA-C*06:02 se considera el principal alelo de riesgo de la psoriasis vulgar. Se localiza en el locus de susceptibilidad a la psoriasis PSORS1. Se aportaron pruebas de la existencia de patomecanismos autoinmunes en la psoriasis al descubrirse que el HLA-C*06:02 provocaba una respuesta autoinmune contra el ADAMTSL5, un autoantígeno melanocítico. Además de ADAMTSL5, LL-37/Cathelicidin y PLA2G4D son otros dos autoantígenos potenciales que parecen desempeñar un papel en el inicio o el mantenimiento de las lesiones psoriásicas.
Los procesos del sistema inmunitario innato y adquirido intervienen en la inmunopatogénesis de la psoriasis. En el inicio de la cascada inflamatoria intervienen células del sistema inmunitario innato. Aquí, las células dendríticas (CD) y los macrófagos parecen desempeñar un papel clave en el establecimiento de una respuesta inmunitaria dominada por las células T helper-1 (Th1) y Th17. La activación de las CD en la piel conduce a la liberación de interleucinas-12 (IL-12) e IL-23, que estimulan a las células T ingenuas a diferenciarse en células Th1 (por la IL-12) y Th17 (por la IL-23).
Las células T helper (Th) coordinan la respuesta inmunitaria adaptativa mediada por células. Las células Th1 y Th17 activadas secretan las citocinas IFN-γ y TNF-α e IL-17 e IL-22, respectivamente, que impulsan la patogénesis posterior. En la psoriasis, la respuesta inmunitaria está mediada principalmente por las células Th1, mientras que en la dermatitis atópica existe una dominancia Th2. Las poblaciones de células T en biopsias de lesiones psoriásicas, que mostraron infiltrados de células T diferentes en comparación con las lesiones en el contexto de la dermatitis atópica en el mismo paciente, confirman el paradigma Th1/Th2.
El TNF-α, el IFN-γ, la IL-17A, la IL-17F, la IL-22 y la IL-6 forman una red de citoquinas en las lesiones psoriásicas que, entre otras cosas, induce la hiperproliferación de los queratinocitos. El proceso de diferenciación acelerado de los queratinocitos acorta su tiempo de tránsito del estrato basal al estrato córneo de unos 30 a 5-8 días. El resultado es la descamación y el engrosamiento de la epidermis típicos de la psoriasis.
Los queratinocitos activados también producen mediadores proinflamatorios y expresan moléculas de adhesión en la superficie celular, lo que conduce a la amplificación y cronificación de la respuesta inmunitaria. Las lesiones psoriásicas presentan un recuento total de células inmunitarias superior al de la piel sana. Incluso en la piel de los pacientes con psoriasis, que clínicamente no presenta lesiones, pudo detectarse un mayor número de células T que en la piel sana. La acumulación intraepidérmica de células CD8 es crucial para el desarrollo de las lesiones psoriásicas.
Tras la presentación de los autoantígenos a las células dendríticas, se produce la activación de las células T. Las células T activadas migran a la epidermis, por lo que son necesarios procesos complejos para entrar en ella; se sospecha que las integrinas α1β1 desempeñan un papel importante en ello. El bloqueo de α1β1 mediante un anticuerpo monoclonal provocó la acumulación de células T epidérmicas y el desarrollo de lesiones psoriásicas en el modelo de ratón.
Las células T, que se localizan en la epidermis, desempeñan un papel extremadamente importante en la patogénesis de la psoriasis. En las placas psoriásicas, las células CD4 positivas se encuentran principalmente en la dermis y las CD8 positivas predominantemente en la epidermis. Una gran proporción de las células CD8 positivas de la epidermis pertenecen a las “células T de memoria residentes en el tejido” (células TRM, CD8+ TRM). Se trata de células T de memoria que permanecen en las lesiones psoriásicas aclaradas y mantienen una memoria inmunológica, lo que explica por qué las lesiones psoriásicas reaparecen a menudo en los mismos sitios. Los TRM CD8+ son un biomarcador potencial de la actividad residual de la enfermedad.
En la década de 1980, los estudios con el inmunosupresor ciclosporina A, que resultó eficaz en el tratamiento de la psoriasis, confirmaron que se trataba de una enfermedad mediada por las células T. La ciclosporina inhibe la fosfatasa calcineurina en el citoplasma y bloquea así la fosforilación del factor nuclear de las células T (NFATc), responsable de la activación de los genes de diversas citocinas proinflamatorias. Los efectos antipsoriásicos de los anti-CD4 y CTLA-4-Ig proporcionaron un apoyo adicional a la tesis de que las células T son una diana terapéutica importante.
En la década de 1990, un grupo de investigación estadounidense demostró que podían inducirse lesiones inyectando células T autólogas en piel psoriásica no enferma injertada en ratones SCID. En el mismo modelo, se demostró que los linfocitos T CD4+ inducen lesiones psoriásicas en piel psoriásica no enferma.
Anticuerpos Monoclonales y Moléculas Pequeñas
Los productos biológicos han revolucionado las opciones de tratamiento de la psoriasis. Con las sustancias activas biológicas disponibles hoy en día, se puede lograr un control de la enfermedad eficaz y seguro a largo plazo. Mientras que el uso de anticuerpos anti-TNF-α puede lograr PASI75# en la mayoría de los pacientes, los anticuerpos anti-IL17A y los anticuerpos anti-IL-23 conducen a PASI100** en aproximadamente la mitad de los pacientes, lo que pone de relieve la relevancia de la vía IL-23/IL-17 en la psoriasis. La eficacia de los biológicos se ha comparado en metaanálisis en red.
Dependiendo de las características del paciente, incluidas las comorbilidades que pueda presentar, es más preferible una u otra clase de sustancia. En Suiza, además de los inhibidores del TNF-α y el anticuerpo contra la IL12-/23 ustekinumab, actualmente están aprobados varios principios activos de los grupos de los anticuerpos anti-IL17A (secukinumab, ixekizumab) y los anticuerpos anti-IL-23 (guselkumab, risankizumab, tildrakizumab) . Y el inhibidor de IL17A/17F bimekizumab también ha superado ahora los obstáculos para su aprobación.
Del campo de las “moléculas pequeñas”, el inhibidor de la PDE-4 apremilast es un fármaco oral aprobado. Además, actualmente se están probando clínicamente el deucravacitinib (TYK2-i oral), el roflumilast (PDE-4-i tópico) y el tapinarof (agonista AHR tópico).
Se sabe que las células CD4+ Th segregan diversas citocinas. La importancia de estas sustancias mensajeras en la patogénesis de la psoriasis queda confirmada por la muy buena respuesta terapéutica con la neutralización dirigida de citoquinas individuales del sistema inmunitario. En primer lugar, se descubrió que el bloqueo del TNF-α ayudaba a aliviar la psoriasis. Posteriormente se aprobó el ustekinumab, un biológico dirigido contra la subunidad p40 común de la IL-12 y la IL-23, que demostró una buena eficacia en la psoriasis. Los anticuerpos monoclonales que se dirigen selectivamente a la subunidad p19 de la IL-23 (guselkumab, risankizumab, tildrakizumab) han demostrado ser aún más eficaces.
Además de las diversas clases de productos biológicos (antagonistas del TNFα-, la IL-17-, la IL-12/23- o la IL-23-) y los terapéuticos sistémicos convencionales (ciclosporina A, metotrexato, acitretina o ésteres del ácido fumárico), los agentes de moléculas pequeñas también desempeñan un papel en la farmacoterapia de la psoriasis. El apremilast es un inhibidor oral de la PDE-4 (fosfodiesterasa-4) que está aprobado para el tratamiento de la psoriasis, entre otras afecciones. Los efectos antiinflamatorios del apremilast se producen por un aumento de los niveles intracelulares de AMPc. Además, actualmente se está probando en ensayos clínicos el Roflumilast, un inhibidor de la PDE-4 de aplicación tópica. Esto también se aplica a otros representantes de las “pequeñas moléculas”.
| Fármaco | Dosis | Vía de Administración | Resultados PASI | Efectos Secundarios |
|---|---|---|---|---|
| Alefacept (Amevive®) | 10-15 mg | Intramuscular semanal | Reducción del 75% en el 33% de los pacientes | Mínimos; no inmunosupresión |
| Siplizumab (MEDI-507) | Variable | Subcutánea semanal | Reducción del 75% en el 39% de los pacientes (dosis alta) | Datos limitados |
| Efalizumab (Xanelim®) | 0.7 mg/kg inicial, luego 1-4 mg/kg semanal | Subcutánea | Mejoría del 50% o más en el 75% de los pacientes | Cefaleas, síntomas gripales |
tags: #anticuerpo #monoclonal #psoriasis