En los últimos años, hemos presenciado un cambio radical en el tratamiento de las neoplasias sólidas y hemáticas. A medida que se ha avanzado en el conocimiento de la biología molecular del cáncer, las posibilidades terapéuticas se han multiplicado incluyendo la quimioterapia combinada, la terapia con citocinas y, más recientemente, el tratamiento biológico dirigido contra subtipos específicos de cáncer.
La terapia dirigida contra dianas neoplásicas tiene dos características fundamentales: su especificidad, que ha conseguido una efectividad significativamente superior a la de otros fármacos disponibles previamente en el mercado, y la capacidad de evitar dañar otras células no relacionadas con la enfermedad neoplásica para así limitar sus efectos secundarios. A pesar de ello, la toxicidad cutánea que presentan algunos de los nuevos fármacos supone un obstáculo para los oncólogos a la hora de completar, a las dosis óptimas, algunos de los protocolos de quimioterapia más recientes. Además, la toxicidad cutánea tiene un impacto físico y emocional muy importante para el paciente y sus cuidadores.
Por otra parte, el mayor conocimiento de estos fármacos podría conducir a la ampliación de las indicaciones terapéuticas en el terreno de la dermatología.
Desde mediados de la década de los noventa se utilizan terapias específicas para diferentes enfermedades malignas. En la actualidad están aprobados nuevos agentes que tienen un mecanismo de acción que difiere completamente del de los antineoplásicos clásicos. Algunos de ellos actúan directamente contra dianas específicas del cáncer, mientras que otros modifican la regulación de vías de señalización que participan en el crecimiento alterado que caracteriza los procesos neoplásicos. Éstos tienen como dianas frecuentes los factores de crecimiento como el factor de crecimiento endotelial (VEGF), las moléculas de señalización intercelular como la ciclooxigenasa 2 o la tirosincinasa BCRABL o los receptores de membrana celular como los miembros de la familia HER, entre los que se incluye HER1/EGFR, que corresponde al receptor del factor de crecimiento epidérmico (EGFR).
Se han descrito 4 receptores de factores de crecimiento epidérmico: HER-1 (epidermal growth factor receptor, EGFR o c-erb B1), HER-2 (c-erb B2), HER-3 (c-erb B3) y HER-4 (c-erb B4).
EGFR se expresa de forma habitual en las células de los distintos tejidos del organismo.
Toxicidad Cutánea por Inhibidores de EGFR (IEGFR)
Los efectos adversos más frecuentemente documentados con los IEGFR (tanto anticuerpos monoclonales como los inhibidores tirosin-kinasa) son los derivados de la toxicidad dermatológica. Ocurre en un 50-100% de los pacientes sometidos a tratamiento, siendo dicha toxicidad más florida con Cetuximab y Panitumumab.
La forma más común de presentación es la llamada reacción papulopustular o rash acneiforme, que afecta al 60-80% de los pacientes. Es generalmente de leve a moderada y severa únicamente en 5-20% de los mismos.
Se define como una erupción dermatológica confinada fundamentalmente a zonas ricas en glándulas sebáceas como son: cara, cuello, zona retroauricular, espalda, parte superior de tórax y cuero cabelludo, pudiendo afectar a otras zonas pero siempre respetando las palmas de las manos y las plantas de los pies.
La erupción es dosis dependiente y tiende a ser más severa, más frecuente y extensa con los anticuerpos monoclonales que con los ITK.
Otros efectos incluyen:
- Xerosis o sequedad cutánea: principalmente en pacientes de edad avanzada, que han llevado tratamiento previo con citotóxicos y que presentan historia de eczema atópico.
- Cambios ungueales: aparecen en el 10-15% de los pacientes y se trata de un evento tardío (raramente aparece antes de las 8 semanas de tratamiento). Se caracterizan porque las uñas tienden a crecer más lentamente, a tener mayor fragilidad y tendencia a romperse.
- Telangiectasia e Hiperpigmentación: como resultado final de la resolución de la erupción acneiforme.
La toxicidad cutánea derivada del uso de IEGFR parece estar relacionada con la respuesta tumoral y la supervivencia del paciente. Por tanto, la aparición del rash y su severidad podría ser un marcador predictivo de la eficacia de los IEGFR.

Manejo de la toxicidad cutánea inducida por inhibidores de EGFR
El objetivo principal del tratamiento de la toxicidad cutánea es aliviar el malestar físico y emocional que sufren los pacientes, en especial aquellos que tienen un peor pronóstico o se encuentran en fases de enfermedad avanzada.
Otras Toxicidades Asociadas a IEGFR
La toxicidad gastrointestinal descrita con los IEGFR es consecuencia del daño producido a nivel de la mucosa del intestino delgado y colon, produciendo un exceso de fluidos secretados en la luz intestinal.
Aproximadamente, el 20 % de los pacientes en tratamiento con Cetuximab van a experimentar una reacción de hipersensibilidad de cualquier grado durante la infusión del fármaco.
Pneumonitis
Toxicidad descrita principalmente con los TKI de EGFR, tanto Gefitinib como Erlotinib. Ocurre típicamente dentro de los primeros 90 días de tratamiento, con una incidencia en torno al 1-2 % en las series Japonesas y una mortalidad en torno al 0.87% y una incidencia del 0,3 % en EEUU.
El manejo de la pneumonitis inducida por drogas (tanto de Gefitinib como Erlotinib) consiste en la interrupción del agente causal y la corticoterapia sistémica. Es importante excluir la causa infecciosa de la pneumonitis antes de iniciar el tratamiento corticoideo, por el efecto inmunosupresor que este ocasiona.
La diarrea asociada a afatinib suele aparecer normalmente durante las primeras dos semanas de exposición al fármaco.
Los acontecimientos adversos cutáneos incluyen exantema, acné, dermatitis acneiforme y sequedad cutánea.
Reconociendo las Erupciones Acneiformes
No te fíes del nombre. Las erupciones acneiformes no están relacionadas con las lesiones de acné: no son ni comedones ni microquistes. Sin embargo, su aspecto es similar al del acné y también su localización: estas manchas rojas, a veces coronadas por una cabeza blanca, aparecen en las zonas de la piel con más glándulas sebáceas, donde la piel es más grasa.
Las erupciones acneiformes (o «brotes») pueden aparecer en la cara, el cuero cabelludo, la parte superior del pecho y la espalda.

Ejemplo de Erupciones Acneiformes
Otros Fármacos Antineoplásicos y sus Efectos Cutáneos
Se revisan los diferentes fármacos antineoplásicos agrupándolos según su mecanismo de acción y el perfil similar de efectos secundarios cutáneos que producen:
Rituximab (Mabthera®)
Con la aprobación de rituximab en 1997 se inició la terapia con anticuerpos monoclonales dirigidos contra dianas específicas involucradas en la fisiopatología del cáncer. Este anticuerpo monoclonal quimérico antiCD20 se introdujo inicialmente para el tratamiento del linfoma no hodgkiniano de células B, y actualmente se utiliza para otras neoplasias, así como para procesos inflamatorios autoinmunitarios.
A pesar de que presenta pocos efectos secundarios cutáneos, se ha descrito un caso de síndrome de Stevens-Johnson asociado a su uso. De la misma forma que con otros anticuerpos monoclonales quiméricos, son frecuentes las reacciones infusionales, que se pueden manifestar con fiebre, cefalea, hipotensión, disnea y erupción cutánea morbiliforme en las 24-48 h posteriores a la primera infusión del fármaco. La enfermedad del suero también puede presentarse con una erupción morbiliforme, de la que se han publicado 2 casos con rituximab. Es más evidente en las zonas acrales, aparece entre la primera y la segunda semana tras la infusión y presenta datos analíticos de consumo de complemento y elevación de reactantes de fase aguda.
Inhibidores de la Tirosincinasa BCR/ABL: Imatinib (Glivec®), Dasatinib (Sprycel®) y Nilotinib (Tasigna®)
El mesilato de imatinib es una pequeña molécula que inhibe la transducción de señales a través de varias tirosincinasas, entre las que se encuentran BCR-ABL, el receptor del factor de crecimiento derivado de las plaquetas (PDGFR) y el gen c-kit. El fármaco está aprobado para el tratamiento de leucemia mieloide crónica positiva para cromosoma Filadelfia, los tumores de la estroma gastrointestinal (GIST) y el síndrome hipereosinofílico.
Se han descrito diversos efectos secundarios cutáneos con imatinib, los más frecuentes de los cuales se recogen en la tabla II. En los ensayos clínicos iniciales, hasta el 60% de los pacientes presentaron edema, y en el 22% apareció una erupción generalizada descrita en la mayoría de los casos como máculas o pápulas eritematosas. En estudios prospectivos posteriores la incidencia de la erupción y el edema alcanzaba el 66,7 y el 65% respectivamente, y se describieron las características clínicas de las lesiones.
En la mayoría de los casos, la erupción es un exantema maculopapular que afecta a la cara, los brazos o el tronco y, con menor frecuencia, las extremidades inferiores, el cuero cabelludo y las áreas intertriginosas. Las lesiones aparecen aproximadamente unos 2 meses tras el inicio del tratamiento, mientras que el edema se inicia unos 15 días antes que las lesiones cutáneas. El edema predomina en la zona de la cara, especialmente en la región periocular, y puede ir asociado a epífora.
También se observa en otros territorios como los tobillos, los antebrazos o cualquier localización con dermis laxa. Este efecto adverso es consecuencia de la retención de líquidos secundaria al fármaco, que puede manifestarse en otros territorios como derrame pleural, insuficiencia cardíaca congestiva, derrame pericárdico, edema pulmonar y ascitis, entre otros. Ambos efectos adversos, la erupción y el edema, dependen de la dosis.
Se ha descrito una incidencia de erupción del 33% con dosis ≤400 mg diarios, mientras que es del 93% con dosis ≥600 mg diarios. Curiosamente, la prevalencia de la erupción es significativamente superior en mujeres.
Aunque en la mayoría de los casos las lesiones cutáneas son leves o moderadas, se han descrito casos de dermatitis exfoliativa, síndrome de Stevens-Johnson y síndrome DRESS (toxicodermia con eosinofilia y síntomas sistémicos) con imatinib. Estas toxicidades cutáneas, incluso en casos extensos, responden favorablemente a la suspensión del fármaco durante un lapso que oscila entre 2 días y 2 semanas. Tras la resolución del cuadro, se puede intentar la reintroducción de imatinib a una dosis menor, combinado con prednisolona oral o no. Las lesiones cutáneas obligan a suspender el tratamiento sólo en un 3% de los pacientes.
El prurito es otro efecto secundario frecuente que suele acompañar a la erupción, aunque también puede aparecer sin lesiones cutáneas en un pequeño porcentaje de pacientes. Otro cuadro clínico relacionado con imatinib es la pustulosis exantemática aguda generalizada (PEAG), que se presenta con fiebre alta, leucocitosis y una erupción pustulosa folicular estéril. En todos los pacientes las lesiones aparecen entre el primer y el tercer mes de tratamiento.
También se ha descrito el desarrollo de síndrome de Sweet en pacientes con leucemia mieloide crónica tras el inicio del tratamiento con imatinib. Las lesiones responden favorablemente al tratamiento con esteroides orales y pueden recurrir o no tras la reintroducción del fármaco. En con-junto, la descripción de casos de PEAG y síndrome de Sweet en relación con imatinib indica una incidencia aumentada de dermatosis neutrofílicas con este fármaco. También se ha descrito un caso de hidradenitis ecrina neutrofílica.
Son frecuentes las alteraciones de la pigmentación, que se pueden manifestar como hiperpigmentaciones, hipopigmentaciones o acromías locales o generalizadas. Tanto la hipopigmentación como la aparición de lesiones acrómicas son más frecuentes en pacientes con fototipos pigmentados y aparecen inmediatamente o hasta 3 meses tras el inicio del tratamiento. En un amplio estudio, Arora et al observaron despigmentación localizada o generalizada en el 41% de los pacientes de una serie de 118 a los 6 meses de tratamiento. El tiempo medio de aparición de las lesiones fue de 4 (2-14) semanas. Desde la aparición, las lesiones progresaban con el tiempo y eran reversibles en caso de reducción o suspensión del tratamiento.
Se ha descrito la imposibilidad para broncearse a pesar de horas de fotoexposición, el aumento en la pigmentación tras la suspensión del tratamiento o la progresión de un vitíligo preexistente. Por el contrario, también se ha descrito la hiperpigmentación paradójica de la piel, así como de las uñas o el pelo, incluso la repigmentación del cabello cano. Además, se ha detectado fotosensibilidad hasta en el 7% de los pacientes con determinación de anticuerpos antinucleares negativos, que afecta especialmente a pacientes de fototipos bajos. Estos hallazgos indican la interacción de imatinib con los melanocitos. En este sentido, varios estudios han demostrado la relación de c-kit con la melanogénesis, la homeostasis de los melanocitos de la piel y la pigmentación inducida por la radiación ultravioleta.
Este hecho podría explicarse por la relación de la mutación de c-kit con el piebaldismo.
Otros efectos secundarios menos frecuentes relacionados con el tratamiento con imatinib son la xerosis, la inducción, exacerbación o mejoría de lesiones de psoriasis, la vasculitis de pequeño vaso, el eritema nudoso y las erupciones tipo reacción de injerto contra huésped. También se han descrito erupciones liquenoides tanto de la piel como de la mucosa oral por imatinib. Existen casos aislados de erupciones del tipo de las micosis fungoides, 1 caso de mucinosis folicular, 4 casos de erupción tipo pitiriasis rosada, 1 caso tipo papuloeritrodermia de Ofugi, 1 porfiria cutánea tardía, 1 siringometaplasia escamosa ecrina y 1 caso de un proceso linfoproliferativo B primario cutáneo relacionado con el virus del Epstein-Barr.
Dasatinib y nilotinib son inhibidores de la tirosincinasa BCR-ABL de segunda generación. Ambas tienen indicación para leucemia mieloide crónica (LMC) con cromosoma Filadelfia positivo en fase crónica o acelerada. El desatinib está indicado además para la crisis blástica de la LMC y la leucemia linfoblástica aguda procedente de LMC, en pacientes que hayan presentado resistencia o intolerancia al tratamiento previo, incluido imatinib.
En los ensayos clínicos iniciales con dasatinib se ha descrito un perfil de efectos adversos cutáneos similar al del imatinib, con erupción cutánea en el 35% de los pacientes, edema superficial en el 36%, edema generalizado en el 5%, inflamación mucosa en el 16% y prurito en el 11%. La erupción se describe como un eritema localizado o generalizado, lesiones maculares o papulares o una erupción exfoliativa. Otros efectos secundarios incluidos en la ficha técnica son hiperhidrosis, alopecia, xerosis, acné, urticaria, fotosensibilidad, hipopigmentación e hiperpigmentación y alteraciones ungueales. También se han descrito en relación con el dasatinib úlceras cutáneas, síndrome de Sweet, enfermedades ampollares, eritrodisestesia palmoplantar y paniculitis.
En los primeros ensayos clínicos disponibles con nilotinib, el 20% de los pacientes presentaban una erupción cutánea leve o moderada; el 15%, prurito; el 12%, xerosis, y el 6%, alopecia. Estos efectos secundarios se presentaron con cualquier posología, aunque la incidencia aumentaba con el aumento de la dosis. En estudios posteriores, la incidencia de erupción cutánea fue del 28% y la de prurito, del 24%.
Indicaciones en dermatología
Es importante destacar que el imatinib se ha utilizado con éxito en el tratamiento del dermatofibrosarco-ma protuberans, especialmente en portadores de la translocación t(17;22), y en un caso de histiocitosis de células no langerhansianas diseminada. También se ha utilizado en el sarcoma de Kaposi, concretamente en el relacionado con la infección por el virus de la inmunodeficiencia humana. A pesar de que no hay estudios con desatinib, se cree que podría ser de utilidad en casos de dermatofibrosarcoma protuberans resistentes a imatinib.
Inhibidores de cinasas de amplio espectro: Sorafenib (Nexavar®) y Sunitinib (Sutent®)
Estos nuevos fármacos tienen la capacidad de inhibir varias vías que permiten la perpetuación del crecimiento tumoral. La activación de la tirosincinasa del receptor del factor de crecimiento del endotelio vascular (VEGFR) origina la unión de factores proangiogénicos y perpetúa la cascada de señales que acaba en la formación de neovasos. La activación de la tirosincinasa del receptor del factor de crecimiento derivado de las plaquetas (PDGFR) conduce al reclutamiento de pericitos, que intervienen en la maduración de los neovasos. Al bloquear la actividad de estos receptores o inhibir algún paso intermedio de sus vías de activación -como la RAF serina/treonincinasa-, se puede detener la formación de vasos que nutren el tumor. Además, sorafenib y sunitinib inhiben c-kit y el receptor 3 de la tirosincinasa relacionada con FMS. Con ello actúan indirectamente inhibiendo la angiogénesis relacionada con el tumor y directamente contra el crecimiento tumoral. Estos fármacos han demostrado efectividad en el tratamiento del carcinoma de células renales. Sorafenib además se utiliza en el carcinoma hepatocelular y sunitinib en el carcinoma de la estroma gastrointestinal. Su eficacia en otras neoplasias está en estudio debido a su amplio espectro de actividad. Desde el punto de vista cutáneo, presentan diferentes efectos adversos.
En la cara pueden aparecer lesiones que recuerdan una dermatitis seborreica, especialmente con sorafenib. Aparecen tras la primera o la segunda semana de tratamiento, pueden precederse o concomitar con una eritrodisestesia del cuero cabelludo y suelen desaparecer tras varias semanas de tratamiento sin necesidad de terapia específica. En general, las lesiones empeoran con el calor. Puede haber edema facial leve o moderado hasta en el 50% de los pacientes en tratamiento con sunitinib. Es más evidente en los párpados y no se asocia a aumento de peso.
El sorafenib induce grados variables de alopecia en la mitad de los pacientes tratados, independientemente de la dosis, sin que se conozca su mecanismo causal. En el 30% de los pacientes con sunitinib y el 60% con sorafenib aparecen hemorragias en astilla 2-4 semanas tras el inicio del tratamiento. No están asociados con fenómenos embólicos, sino que se postula que son secundarios a fallo en la renovación de los capilares debido a la inhibición de VEGFR en zonas sometidas a microtraumatismos constantes.
La coloración amarillenta transitoria de la piel y la orina debido a la excreción del fármaco y sus metabolitos aparece tras la primera semana de tratamiento con sunitinib.
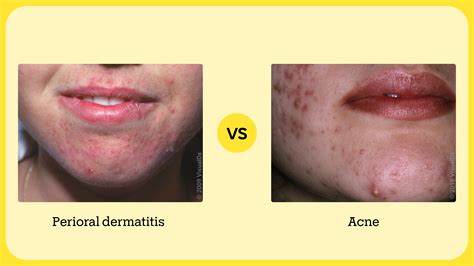
Dermatitis Perioral
Dermatitis Perioral: Un Caso Común
Últimamente, numerosas celebrities están mostrando su cara más humana al hablar de enfermedades que padecen. En este post os hablaremos de uno de esos casos, el de Haiely Bieber, que sufre desde hace varios años dermatitis perioral. Y como en FEMM contamos con un servicio de dermatología, hemos pedido a nuestra dermatóloga, la Dra.
Estas lesiones pueden ser asintomáticas, pero también pueden causar escozor, irritación e incluso descamación. No se transmite por contacto y comparte algunos síntomas, como granitos, enrojecimiento de la zona afectada o escamas, con otras enfermedades de la piel como la rosácea, el acné, la dermatitis por contacto o el herpes zóster. Se calcula que esta enfermedad se da cada año en el 0,5-1% de las personas en el mundo desarrollado, y es más frecuente en niños y en mujeres en edad fértil, aunque puede afectar a cualquier edad y raza.
Hailey señalaba en su post que la dermatitis se la ha provocado el uso y abuso de diferentes productos de belleza. La Dra. Los corticoides inhalados que emplean los pacientes asmáticos también pueden estar en el origen de la dermatitis perioral.
En cuanto al tratamiento, la Dra. Generalmente, como punto de partida, hay que dejar de usar el producto que la esté causando, ya sean cosméticos, solares o cremas con corticoides. También puede emplearse metronidazol tópico, que sirve para tratar infecciones provocadas por determinadas bacterias, o los inhibidores tópicos de la calcineurina. En casos más severos, la Dra.
Habitualmente, los tratamientos indicados se administran durante varias semanas, hasta que la erupción remite.
CÓMO ELIMINAR GRANOS ALREDEDOR DE LA BOCA | DERMATITIS PERIORAL ¿POR QUÉ SALE? DIFERENCIA CON ACNÉ
tags: #dermatitis #acneiforme #tratamiento