La psoriasis es una enfermedad cutánea inflamatoria crónica que cada vez se reconoce más como una enfermedad sistémica. Además de los síntomas cutáneos típicos, los afectados a menudo presentan síntomas acompañantes en otros sistemas de órganos, especialmente en el intestino. Esta conexión plantea nuevas preguntas sobre la fisiopatología y posibles enfoques terapéuticos.
Estudios sugieren que los pacientes con psoriasis tienen un mayor riesgo de enfermedades intestinales inflamatorias como enfermedad de Crohn o colitis ulcerosa. Sin embargo, incluso sin enfermedades intestinales manifiestas, muchos afectados experimentan síntomas como flatulencia, dolor abdominal o diarrea.
Nuevos Hallazgos sobre Inflamaciones Intestinales Subclínicas
Un estudio reciente examinó el intestino de pacientes con psoriasis sin enfermedades intestinales visibles. Se encontraron cambios significativos en la mucosa intestinal.
En particular, el número de células inmunitarias activadas como los granulocitos eosinófilos, los macrófagos y las células T CD8+ fue mayor en comparación con los controles sanos. Además, aproximadamente la mitad de los pacientes con psoriasis tenían una permeabilidad intestinal aumentada. Esta alteración de la permeabilidad se correlacionó con niveles elevados de citocinas (incluyendo IL-17A e IL-13) y síntomas gastrointestinales.
- Granulocitos eosinófilos: La densidad de estas células inmunitarias fue significativamente mayor en el duodeno de pacientes con psoriasis. Además, mostraron marcadores de actividad aumentada como CD66b, que indican activación celular y degranulación.
- Mastocitos: Se encontró un mayor número de mastocitos en el duodeno, pero sin evidencia de una actividad aumentada.
- Macrófagos: Los investigadores observaron un cambio hacia macrófagos proinflamatorios M1, que son conocidos por su papel en las inflamaciones crónicas.
- Células T CD8+: Estas células no solo estaban aumentadas, sino que también mostraron marcadores de actividad elevada como CD69 y CXCR3. Esto sugiere un papel central en el proceso inflamatorio.
¿La Barrera Intestinal Alterada como Fuente de Inflamación?
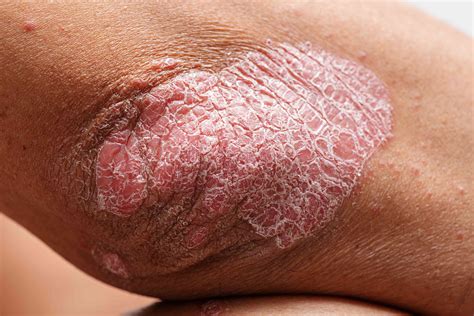
La barrera intestinal juega un papel central en la protección contra microorganismos patógenos y toxinas. Una permeabilidad aumentada, como se observó en los pacientes estudiados, podría promover la entrada de mediadores inflamatorios en el sistema circulatorio sistémico.
La consecuencia: reacciones inflamatorias subclínicas, pero sistémicas, que no solo afectan el intestino, sino también otros órganos. Es especialmente notable la correlación entre la función de barrera alterada y los síntomas como flatulencia o dolor abdominal, incluso sin una enfermedad intestinal visible.
Enfoque en la Salud Intestinal Necesario
El estudio destaca que la psoriasis debe entenderse como una enfermedad sistémica en la que la salud intestinal juega un papel importante. Los hallazgos sugieren que la estabilización de la barrera intestinal o la modulación inmunológica específica en el intestino podrían desempeñar un papel en la terapia en el futuro.
La psoriasis afecta al 2,3 % de la población española, incidiendo por igual en ambos sexos. Entre las enfermedades gastrointestinales, la psoriasis se asocia a una mayor incidencia de enfermedad inflamatoria intestinal (enfermedad de Crohn o colitis ulcerosa) y enfermedad celíaca, así como de determinados cánceres (esófago, estómago y páncreas).
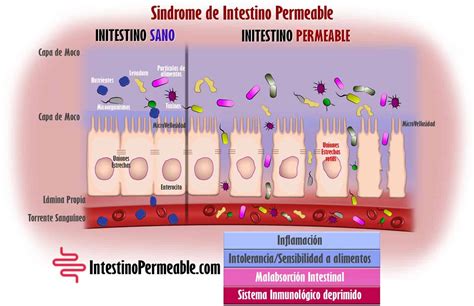
La denominación Enfermedad Inflamatoria Intestinal, que se abrevia frecuentemente como EII, se emplea para referirse a una serie de problemas que afectan predominantemente al intestino y que se caracterizan por producir una inflamación crónica de origen autoinmune que no tiende a la curación. La EII se divide en 2 enfermedades: la enfermedad de Crohn y la colitis ulcerosa. Estas son enfermedades inflamatorias que cursan en brotes y que tienden a la cronificación, y que afectan el tracto gastrointestinal con episodios de inflamación con dolor y diarrea, con potenciales complicaciones graves, como perforación intestinal o sepsis.
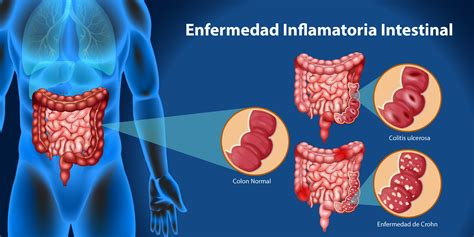
Uno de los principales mecanismos comunes entre la psoriasis y las EII es la activación de la inmunidad innata y adaptativa. En ambas patologías se ha observado una activación de las células T, especialmente las células Th17 y Th1, que juegan un papel crucial en la liberación de citocinas proinflamatorias, como la interleucina-17 (IL-17) y el factor de necrosis tumoral alfa (TNF-α). Además, la microbiota intestinal parece desempeñar un rol fundamental en la regulación de estas enfermedades. En individuos con psoriasis y EII, se ha encontrado una alteración en la composición de dicha microbiota, lo que puede aumentar la permeabilidad intestinal y contribuir a la inflamación sistémica.
La predisposición genética también desempeña un papel en la relación entre psoriasis y EII. Variantes genéticas en ciertos loci (regiones de un cromosoma), como el HLA-Cw6, han sido asociadas tanto con la psoriasis como con la enfermedad de Crohn. Además, el gen IL23R, que codifica el receptor de la interleucina-23, está implicado en la regulación de la respuesta de las células Th17, y se ha relacionado tanto con la psoriasis como con las EII.
Es común que las personas con psoriasis presenten síntomas gastrointestinales, mientras que los pacientes con EII pueden manifestar síntomas cutáneos. Estudios epidemiológicos muestran que los pacientes con psoriasis tienen un mayor riesgo de desarrollar EII en comparación con la población general. En un estudio de cohorte, se observó que el riesgo de desarrollar enfermedad de Crohn en pacientes con psoriasis era aproximadamente 1.7 veces mayor, mientras que el riesgo de colitis ulcerosa era aproximadamente 1.3 veces mayor.
El manejo de estas comorbilidades requiere una atención multidisciplinaria, ya que algunos tratamientos pueden ser efectivos para ambas enfermedades. Por ejemplo, los inhibidores del TNF-α, como el infliximab y el adalimumab, han mostrado eficacia en el tratamiento tanto de la psoriasis como de las EII.
En conclusión, la relación entre psoriasis y EII se basa en mecanismos inmunológicos y genéticos compartidos, de manera que su coexistencia en los pacientes requiere de un manejo cuidadoso.
Desgaste-Reparación (Crohn-Psoriasis)
Psoriasis y Enfermedad del Hígado Graso No Alcohólico (EHGNA)
Entre las enfermedades hepáticas, la psoriasis se relaciona, sobre todo, con la enfermedad del hígado graso no alcohólico (EHGNA) y también con la hepatitis autoinmune. Múltiples estudios epidemiológicos señalan una prevalencia significativamente mayor de EHGNA en los pacientes con psoriasis, siendo esta más del doble que en la población general. Ambas enfermedades comparten en su patogenia el estado de inflamación crónica, la resistencia periférica a la insulina y el síndrome metabólico. Además, esta coexistencia es sinérgica. El síndrome metabólico es más intenso cuando ambas enfermedades están presentes que cuando acontecen por separado.
El dermatólogo es el médico que primero tiene que detectar EHGNA en los pacientes con psoriasis, prestando especial atención a los pacientes con psoriasis moderada o grave que presenten factores de riesgo de síndrome metabólico, independientemente de que tengan alteración de la bioquímica hepática o no, pues podemos estar ante un paciente con EHGNA, incluso grave, con cifras de transaminasas normales o poco elevadas. Las alteraciones de la bioquímica hepática, cuando están presentes, suelen ser leves, con elevación de las transaminasas por debajo de 2-3 veces los valores normales y con un cociente alanino-aminotransferasa (ALT)/aspartato-aminotransferasa (AST) mayor de 1. A veces, se observa una leve elevación de la fosfatasa alcalina y la γ-glutamil-transpeptidasa (GGT).
En relación con el tratamiento del paciente con EHGNA y psoriasis, en primer lugar deben darse recomendaciones generales, como perder peso, realizar ejercicio físico y evitar las bebidas alcohólicas. También deben evitarse las grasas saturadas y las bebidas edulcoradas con fructosa, siendo recomendable el consumo de café. En cuanto al tratamiento sistémico de la psoriasis, es muy importante una correcta elección del fármaco. La acitretina y la ciclosporina producen alteración de la bioquímica hepática en el 25 % y 7 % de los pacientes, respectivamente. El metotrexato en pacientes con psoriasis presenta un riesgo aumentado de hepatotoxicidad. Este fármaco está contraindicado en pacientes con enfermedad hepática grave. Si esta es leve, puede usarse con precaución y estrechos controles. El apremilast no desarrolla apenas hepatotoxicidad y la radiación ultravioleta no ocasiona daño hepático. Los fármacos biológicos anti-TNF -como infliximab, etanercept o adalimumab- son seguros en pacientes con enfermedad hepática. El principal efecto hepatotóxico de estos fármacos es el desarrollo de hepatitis autoinmune.
| Factor de Riesgo de Síndrome Metabólico |
|---|
| Obesidad abdominal |
| Hipertensión arterial |
| Dislipidemia (niveles elevados de triglicéridos y/o niveles bajos de colesterol HDL) |
| Resistencia a la insulina |
| Niveles elevados de glucosa en sangre en ayunas |
Psoriasis y Enfermedad Celíaca
La sospecha del nexo entre la enfermedad celíaca y la psoriasis se basa en evidencias serológicas y epidemiológicas. Desde el punto de vista serológico, se han observado niveles elevados de anticuerpos antigliadina, antiendomisio y antitransglutaminasa en pacientes con psoriasis. Además, también se ha visto que el nivel de estos anticuerpos se correlaciona con la gravedad de la psoriasis. Desde el punto de vista epidemiológico, se ha publicado una mayor prevalencia de enfermedad celíaca en pacientes con psoriasis que en la población general. No obstante, en caso de existir, esta relación podría explicarse por varios mecanismos. En primer lugar, la malabsorción asociada a la enfermedad celíaca puede dar lugar a un déficit de vitamina D, deficiencia que predispone al desarrollo de psoriasis. En segundo lugar, desde el punto de vista inmunológico, en la patogenia de la enfermedad celíaca, además de respuesta Th2 también se observan células Th1 y Th17, implicadas en el desarrollo de la psoriasis. En tercer lugar, también se ha encontrado una relación a nivel genético, al identificarse en ambas enfermedades susceptibilidad genética en ocho genes que regulan la respuesta inmunitaria innata y adaptativa.
Se debe solicitar analítica completa con la determinación de anticuerpos antigliadina, antiendomisio y antitransglutaminasa. Ante la sospecha o diagnóstico de enfermedad celíaca debe derivarse al paciente al gastroenterólogo. El tratamiento consiste en seguir una dieta exenta de gluten.
Psoriasis Paradójica Inducida por Anti-TNF
En los últimos años se han descrito diversos efectos secundarios de los fármacos inhibidores del factor de necrosis tumoral alfa (TNFα), entre los cuales se encuentra el desarrollo, que resulta paradójico, de psoriasis o exantemas psoriasiformes.
Desde el año 2003 se han publicado diversos casos que describen la aparición de psoriasis en pacientes tratados con anti-TNF. Dado que estos fármacos han demostrado su efectividad en el tratamiento de la psoriasis vulgar y la artritis psoriásica, resulta paradójico que se los haya relacionado con el desarrollo de lesiones psoriasiformes, muchas de ellas con componente pustular.
La fisiopatología subyacente a este proceso permanece todavía sin aclarar, aunque todo parece indicar que el interferón alfa (IFNα) tiene un papel esencial. El TNFα regula la producción de IFNα, de hecho, la neutralización del TNF aumenta la producción de IFNα por parte de las células dendríticas plasmocitoides (PDC) y aumenta la expresión de receptores de citocinas, como CXCR3 en las células T circulantes, promoviendo la migración hacia la piel de estas células autorreactivas. Según estos hallazgos, se ha propuesto que la inhibición del TNF produciría una expresión tisular aberrante de IFNα en individuos predispuestos.