La psoriasis es una enfermedad dermatológica frecuente que afecta a millones de personas en el mundo, caracterizada por la aparición de lesiones en forma de placas escamosas o sobreelevadas en la piel.
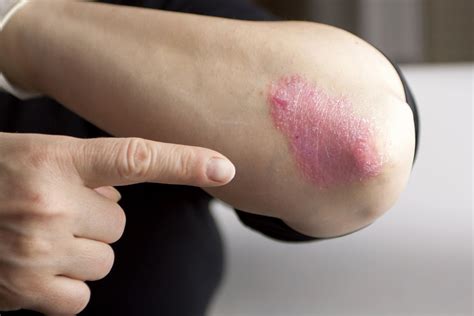
Aunque su impacto visible ocurre en la piel, el origen de la psoriasis radica en el sistema inmunológico. En términos generales, las lesiones suelen ser escamas gruesas y blanquecinas, típicamente localizadas en el cuero cabelludo, codos, rodillas y espalda.
¿Qué es la Psoriasis?
La psoriasis es una enfermedad inflamatoria de la piel con exacerbaciones y remisiones, sin ser contagiosa, que sigue un curso crónico. No es hereditaria pero requiere una predisposición genética para padecerla además de otros factores desencadenantes.
Comienza en el sistema inmune, los linfocitos “T” se activan indebidamente y desencadenan muchas respuestas celulares, una de ella es la proliferación y dilatación de los vasos sanguíneos de la piel (color rojo de las lesiones), otra sería la proliferación de las células de la epidermis “QUERATINOCITOS”.
Clásicamente, se consideraba solo una enfermedad cutánea, y se decía que afectaba a las articulaciones en un 30% de los casos, pero hasta ahí se llegaba. Sin embargo, desde hace algunos años la consideramos una enfermedad inflamatoria sistémica porque se asocia con otras enfermedades que tienen un perfil inmunológico similar”.
Entonces, no es solo la artritis; también se asocia con enfermedades inflamatorias intestinales, inflamación de los ojos y un riesgo cardiovascular importante. Quienes padecen psoriasis más severa tienen un mayor riesgo de desarrollar hipertensión, dislipemia y diabetes, y existen estudios que confirman que la esperanza de vida de pacientes con psoriasis cutánea severa es más corta.
Esta manera más integral de ver la enfermedad ha permitido observar que hay una conexión con otras condiciones de salud. “Antes pensábamos que era solo una enfermedad de la piel, pero ahora comprendemos su relación con muchas otras áreas”. Este nuevo abordaje que amplía el foco de atención está dando muy buenos resultados, aumentando la calidad y esperanza de vida, para pacientes de psoriasis también.
La Autoinmunidad en la Psoriasis
Una enfermedad autoinmune se define clásicamente por la presencia de autoantígenos pero también por la producción de autoanticuerpos por los linfocitos B transformados para la ocasión en plasmocitos secretores de anticuerpos.
Un ejemplo de enfermedad autoinmune es el lupus, donde autoanticuerpos de tipo anti-ADN nativo causan inflamación y lesiones orgánicas a nivel cutáneo, articular, cardíaco, renal, neurológico…
Por ahora no se han encontrado autoanticuerpos en la fisiopatología de la psoriasis, pero eso no nos impide hablar de autoinmunidad en la psoriasis puesto que las propias células inmunitarias del individuo, y, en particular, los linfocitos T, reaccionan de forma exagerada ante los autoantígenos, cuando deberían tolerarlos, ¡no atacarlos!
A la espera de obtener una respuesta clara sobre los mecanismos fisiopatológicos de la psoriasis, digamos simplemente que la psoriasis es una enfermedad inflamatoria crónica con una fuerte implicación de los propios recursos inmunitarios del individuo, de ahí que los distintos tratamientos inmunomoduladores o incluso inmunosupresores recetados por el dermatólogo resulten eficaces.
Tipos de Psoriasis
Su manifestación clínica más habitual es la aparición de lesiones cutáneas de tamaño variable enrojecidas y recubiertas de escamas blanquecinas de grosor variable y que se acumulan debido a su proliferación acelerada.
- Psoriasis vulgar: Constituye la forma más frecuente y se caracteriza por placas rojas bien delimitadas que pueden medir desde pocos milímetros hasta varis centímetros de diámetro. Por lo general las placas se localizan en rodillas, codos, y zona sacra, aunque pueden aparecer en cualquier parte del cuerpo.
- Psoriasis palmoplantar: Se caracteriza por placas muy secas e hiperqueratosicas y puede interferir mucho en el trabajo y en la vida personal, porque la piel suele agrietarse, sangrar y doler.
- Psoriasis del cuero cabelludo: Es muy frecuente, puede ser la forma de inicio o la única localización de la enfermedad, se presenta en forma de descamación seca muy adherida, sobre una zona roja del cuero cabelludo. En ocasiones las lesiones se extienden hacia la frente, la nuca o detrás de las orejas, suele producir mucho picor.
- Afección de las uñas: La afección es muy variable (entre un 20%-40% de los enfermos) , algunos no la tienen, otros tienen pequeños puntos, otros tienen engrosamientos y deformación de las uñas y otros manchas amarillas correspondientes al despegamiento del lecho ugueal.
- Psoriasis guttata: Este tipo de psoriasis recibe esta denominación porque las lesiones son pequeñas, menores de 2 cm. , numerosas y distribuidas de forma irregular por todo el cuerpo, como una salpicadura. Es más frecuente en niños y jóvenes y suele aparecer tras una infección por estreptococo, gereralmente una faringo-amigdalitis.
- Psoriasis eritrodérmica: La piel se encuentra muy roja, caliente y descamación de forma abundante.
- Artritis psoriásica: Es una forma de inflamación crónica de las articulaciones que se caracteriza por rojez, hinchazón y dolor de las articulaciones afectadas. Comienza entre los 30-50 años, y entre un 10%-30% de las personas que tienen psoriasis desarrollan artritis. En ocasiones la afectación articular aparece meses o años antes que las lesiones cutáneas.
¿Qué es psoriasis? Causas, síntomas y tratamiento
Inmunopatogénesis de la Psoriasis
En la década de 1970 la psoriasis era reconocida como un trastorno hiperproliferativo, por lo que se postuló que la alteración en la proliferación y diferenciación epidérmica era la causa principal de las lesiones psoriásicas.
Posteriormente en 1980 se describió la relación de esta enfermedad con los linfocitos Th1 productores de IFN-γ8. En el último decenio, nuevas evidencias implican a los linfocitos Th17, los macrófagos y las DC en la inducción y el mantenimiento de la psoriasis.
La aparición de psoriasis en receptores de trasplantes hematopoyéticos de donantes afectados y la efectividad de tratamientos inmunosupresores como la ciclosporina, llevó a proponer el papel central del sistema inmune en la generación de la enfermedad8. Sin embargo, todavía no se ha establecido si la primera anormalidad en la psoriasis está en la piel o en el sistema inmune9,10.
Actualmente se acepta que la enfermedad resulta de una anormalidad intrínseca en los queratinocitos epidérmicos y de la activación del sistema inmunológico tanto innato como adaptativo11.
Se reconocen 3 fases en la enfermedad:
- Fase de sensibilización: Después de señales innatas recibidas a través de los receptores tipo Toll (toll like receptor [TLR]) o receptores para las proteínas de choque térmico (heat shock proteins [HSP]), las DC maduran y migran a los órganos linfoides secundarios donde presentan el antígeno a las células T CD4+ vírgenes, las activan y determinan el fenotipo Th1 y Th17 efector y de memoria. En esta fase no hay lesiones visibles en piel.
- Fase silente: Tiene una duración variable y no hay lesiones visibles en piel. Las células T de memoria recirculan por el compartimento linfoide y los tejidos.
- Fase efectora: Esta fase comienza con la infiltración de la piel por varias células inmunes como macrófagos, DC, células T y neutrófilos, generándose mecanismos efectores de la inmunidad innata y adaptativa. En esta fase se presenta inflamación, angiogénesis y una respuesta hiperproliferativa de los queratinocitos.
El inicio de la enfermedad es mediado a través de DC que presentan antígenos extraños o propios aún no identificados a los linfocitos T12. Algunos estudios han indicado que la queratina 17 (K17) es altamente expresada en lesiones psoriásicas y algunos epítopes de K17 son homólogos de la secuencia de la proteína M de estreptococo13.
En este sentido, se conoce que la infección estreptocócica precede a la psoriasis en más del 90% de pacientes con psoriasis tipo I14. Además, las infecciones o daños de la piel pueden promover la formación de lesiones en individuos susceptibles, y se ha demostrado que estos desencadenantes estimulan en los queratinocitos la producción de péptidos antimicrobianos como catelicidina (LL-37) formando complejos con fragmentos de ADN propio reconocidos por TLR-9 en las DC7,15.
Se considera entonces, que el ADN del hospedero se convierte en un estímulo proinflamatorio que rompe la tolerancia inmunológica, conduciendo a la psoriasis7.
La activación de la célula T virgen requiere de la producción de IL-12 por las DC, induciéndose una polarización hacia una respuesta tipo Th1, la cual también requiere de la presencia del IFN-γ. A su vez, los linfocitos Th1 (CD4+ y CD8+) producen IFN-γ, TNF-α e IL-216.
De otro lado, las citocinas IL-1β, IL-6 e IL-23 inducen el desarrollo de los linfocitos Th17. Estas células producen principalmente IL-17, IL-21 e IL-2217. La IL-23 es producida por DC y macrófagos, y es necesaria para el crecimiento, la supervivencia y las funciones efectoras de las células Th17.
Tanto la IL-23 como las células Th17 han sido encontradas de forma abundante en las lesiones psoriásicas6,7. Además, se ha identificado en la epidermis psoriásica la presencia de células T CD8+ que producen IL-17 (Tc17)7.
Ambos tipos de linfocitos T (CD4+ y CD8+) están presentes en la piel psoriásica: mientras los CD4+ infiltran principalmente la dermis, los CD8+ están preferencialmente en la epidermis14. Aunque ambos poblaciones de linfocitos están presentes, las células T CD4+ parecen jugar un papel crítico en la patogénesis de la psoriasis18.
Además de los linfocitos T, los macrófagos son predominantes en el infiltrado inflamatorio localizado en la dermis superficial cerca de la papila dérmica. Los macrófagos son una de las fuentes principales de TNF-α. También se pueden encontrar mastocitos que producen grandes cantidades de TNF-α, IFN-γ e IL-8, y pueden liberar mediadores almacenados en cuestión de minutos y crear rápidamente un entorno necesario en la respuesta innata para el reclutamiento de neutrófilos y linfocitos T14.
Además de la activación persistente de células inflamatorias, se ha reportado alteración en los mecanismos reguladores de la respuesta inmunológica. Aunque ciertos estudios han indicado que el número de células T reguladoras no está alterado en las lesiones psoriásicas, parece haber un defecto en su actividad supresora19; además, la IL-10, una importante citocina reguladora, está disminuida en la psoriasis18.
Principales citocinas implicadas en la psoriasis y sus funciones
| Citocina | Función |
|---|---|
| IL-12 | Polarización hacia respuesta Th1 |
| IFN-γ | Producido por linfocitos Th1, activa células inmunes |
| TNF-α | Inflamación, angiogénesis |
| IL-1β, IL-6, IL-23 | Inducen desarrollo de linfocitos Th17 |
| IL-17, IL-21, IL-22 | Producidas por células Th17, inflamación |
Aspectos Genéticos de la Psoriasis
Se ha propuesto que la psoriasis es una enfermedad compleja de naturaleza poligénica. Estudios en gemelos monocigóticos han mostrado una concordancia con la enfermedad del 70-72%, mientras que la concordancia entre gemelos dicigóticos varía del 15 al 23%, indicando la importancia, tanto de la asociación genética como de aspectos ambientales de naturaleza desconocida1.
La naturaleza autoinmune de la psoriasis se sugirió a partir de su asociación con el complejo human leukocyte antigen (HLA) durante los años 1970. Primero se reportó asociación con el HLA-B13. Posteriormente, fuertes asociaciones fueron identificadas con Cw6 y DR7 en las poblaciones finlandesa y alemana1. Sin embargo, solo el 10% de las personas que expresan HLA-Cw6 desarrollan psoriasis, lo que indica un papel importante de los factores ambientales y genes adicionales5.
Por otro lado, estudios de asociación utilizando barrido genómico (GWAS) han mostrado al menos 10 regiones cromosómicas con vinculación estadísticamente significativa denominadas regiones de susceptibilidad a psoriasis (PSORS1-PSORS10).
El mayor determinante genético es PSORS1, el cual está localizado en el cromosoma 6 e incluye la región del complejo mayor de histocompatibilidad y representa hasta el 35% de la heredabilidad de la enfermedad5. Los genes candidatos localizados en PSORS1 incluyen genes localizados dentro de la región HLA, dentro de la cual el candidato más fuerte es Cw0602, particularmente en el caso de la psoriasis tipo I.
Las personas con HLA-Cw6 tienen un riesgo relativo 10 veces mayor de enfermedad. En esta misma región se encuentra el gen para la corneodesmosina, que codifica para una proteína de adhesión de los queratinocitos, la cual durante la maduración de la capa córnea se somete a una serie de divisiones requeridas para la descamación21.
Además de lo anterior, se han reportado polimorfismos de nucleótido único (single nucleotide polymorphism [SNP]) asociados a la psoriasis en genes que codifican citocinas, receptores y moléculas de señalización como IL-23R, IL-23A, IL-12B, ZNF313 y PTPN2218.
Importancia de la Regulación Epigenética en la Psoriasis
Los cambios cromosómicos que son heredables, pero que no envuelven alteraciones en la secuencia del ADN, son conocidos como modificaciones epigenéticas. El perfil epigenético es altamente dinámico y reversible, y varía entre las células en el mismo organismo y en la misma célula, entre varios estados, tales como la salud versus enfermedad, o en respuesta a las perturbaciones ambientales.
La evidencia ha demostrado que los desequilibrios epigenéticos son elementos causales en varias enfermedades importantes, incluyendo el cáncer y las enfermedades autoinmunes22.
Los mecanismos epigenéticos se consideran el puente entre los factores genéticos y ambientales en la patogénesis de la psoriasis23. Los 3 principales mecanismos de modificaciones epigenéticas son: metilación del ADN, modificación postranscripcional de las histonas y regulación por pequeñas moléculas de ARN no codificantes (nc-ARN)24.
En esta revisión nos centraremos en los nc-ARN, específicamente en los mi-ARN y su papel en la psoriasis con compromiso cutáneo.
ARN reguladores
Uno de los avances más importantes para el entendimiento del control de la expresión génica fue el descubrimiento de moléculas de ARN que regulan la expresión de genes. A finales de 1990 los estudios realizados por Andrew Fire y Craig Mello demostraron que la expresión génica podía ser inhibida por la introducción de ARN de doble cadena con secuencias complementarias al gen blanco, un mecanismo que fue denominado ARN de interferencia (ARNi)28.
Lin-4 fue el primer ARN de interferencia descubierto en el nemátodo Caenorhabditis elegans29. Desde su descubrimiento en el 2001, más de 1.400 ARNi han sido identificados en humanos30. Se han descrito varias clases de moléculas pequeñas de ARN que desencadenan este proceso de silenciamiento por interferencia. Dentro de estas las más conocidas son los ARN pequeños de interferencia (si-ARN) y los mi-ARN28.
Los si-ARN pueden ser endógenos o exógenos, pueden ser codificados en el genoma o ser introducidos exógenamente a través de infecciones virales o mediante transgénesis. Los si-ARN endógenos pueden ser generados a partir de 2 transcritos separados pero complementarios, por ejemplo, a partir de la transcripción bidireccional del mismo locus, los cuales son posteriormente procesados para formar si-ARN. Aunque sus funciones no se conocen completamente, se han asociado con protección contra infecciones virales28.
Los mi-ARN, aunque presentan mucha similitud con los si-ARN, son producidos en parte por una vía de síntesis diferente y son transcritos a partir de genes celulares31. Los mi-ARN son un grupo de ARN pequeños de aproximadamente 20 a 22 nucleótidos (nt) no codificantes, y median la regulación postranscripcional. Los genes que codifican los mi-ARN pueden ser encontrados dentro de los intrones de genes codificantes y no codificantes, dentro de los exones de genes no codificantes y reg...
Tratamientos para la Psoriasis
El objetivo será limpiar o aclarar las lesiones de la piel durante un periodo lo más largo posible “blanquear”. Los medicamentos lo consiguen reduciendo la inflamación y frenando la proliferación de los queratinocitos de la epidermis.
Si la afección es leve se indicará un tratamiento tópico. Si es de leve a moderada y los tratamientos tópicos no son efectivos se puede recomendar la exposición a la luz ultravioleta (fototerapia) o el tratamiento sistémico ( medicamentos orales, subcutáneos, intramusculares o intravenosos).
El criterio es usar primero los tratamientos con menos efecto secundarios y pasar a los más agresivos si los primeros fracasan.
- Climatoterapia y Balneoterapia: El clima seco y fria favorece los brotes de psoriasis y que las placas estén más secas y sean más molestas; mientras que un clima húmedo y caluroso suele mejorarlas, al estar las placas más hidratadas.
- Tratamientos sistémicos: Son los tratamientos administrados por vía oral o los que se inyectan debajo de la piel, en músculo o en vena. Estos tratamientos se indican en la psoriasis moderada o intensa.
- Tratamientos biológicos: Son una forma de tratamiento sistémico con distinto mecanismo de acción. A diferencia de los tratamientos convencionales, los tratamientos biológicos son más eficaces, y sus efectos secundarios son menores. No producen toxicidad orgánica, es decir, no dañan el hígado ni el riñón ni otros órganos. A corto y medio plazo son tratamientos seguros y eficaces, pero a largo plazo se desconoce su seguridad (actualmente se conoce una experiencia en uso de 10-15 años). Este tipo de tratamiento no se puede utilizar en personas con antecedentes de cáncer, de infecciones activas, de tuberculosis o enfermedad neurológica.
En ocasiones y en algunas personas, es posible es posible que las terapias alternativas (acupuntura, homeopatia, aromatoterapia, flores de bach, reflexoterapia, drenaje linfático, etc) produzcan un efecto placebo o psicológico beneficioso que conlleve una mejoría de la enfermedad, pero no existen trabajos científicos que avalen estos procedimientos.
Recomendaciones Adicionales
Las últimas investigaciones apuntan que las personas que padecen una psoriasis intensa e iniciada antes de los 20 años tienen un mayor riesgo de padecer a partir de los 65 años enfermedades como diabetes, hipertensión, obesidad, enfermedades cardiovasculares y artritis entre otras. Para evitar esta situación, debida a la inflamación crónica que provoca la psoriasis grave mal controlada, es aconsejable mantenerla bajo control mediante un tratamiento efectivo y continuo.
Es aconsejable no fumar, no beber alcohol, mantener el peso ideal y realizar ejercicio físico.
Cuando se tiene una enfermedad crónica como la psoriasis, lo más importante es aprender a convivir con ella: aceptarla y tener actitud proactiva. Asimismo informarse e implicarse en el tratamiento resultan de gran ayuda y facilita su cumplimiento.
tags: #psoriasis #y #sistema #inmunologico